
【题目】A、B、C三种物质的溶解度曲线如图。请回答下列问题。
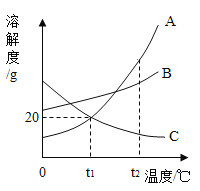
(1)t1℃时,A物质的溶解度是_____g。
(2)保持温度不变将B的不饱和溶液转化为饱和溶液,可采用的一种方法是_____。
(3)将t2℃时等质量A、B、C三种物质的饱和溶液降温至t1℃,所得溶液中溶剂质量最少的是_____。
(4)t1℃时将A、B、C三种物质各5g分别加入20g水中充分溶解,所得溶液质量的大小关系为_____。
【答案】20 增加溶质 A B>A=C
【解析】
(1)通过分析溶解度曲线可知,t1℃时,A物质的溶解度是20g;
(2)保持温度不变将B的不饱和溶液转化为饱和溶液,可采用的一种方法是增加溶质;
(3)t2℃时,A物质的溶解度最大,等质量A、B、C三种物质的饱和溶液中,A物质中的溶剂最少,降温至t1℃,不会影响溶剂的质量,所以所得溶液中溶剂质量最少的是A;
(4)t1℃时,B物质的溶解度最大,A、C物质的溶解度相等,所以将A、B、C三种物质各5g分别加入20g水中充分溶解,由溶解度曲线知,B可能仍未达到饱和,也可能饱和,AC已经饱和且有晶体未全部溶解,所以所得溶液质量的大小关系为B>A=C。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】下列应用及相应原理(用化学方程式表示)都正确的是( )
A. 用稀盐酸除铁锈Fe2O3+6HCl=2FeCl2+3H2OB. 用二氧化碳制碳酸饮料CO2+H2O=H2CO3
C. 用电解水的方法测定水的组成2H2O=2H2↑+O2↑D. 用氢氧化钠制碳酸钠CaCO3+NaOH=Ca(OH)2 + Na2CO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据不同的实验内容回答对应的问题。
实验内容 | 回答问题 |
(1)探究氧气的性质 | ①铁丝表面有铁锈,影响了反应的进行,我们应该___________________________。 ②点燃火柴后不能立即伸入瓶内,因为____ ③该反应的化学方程式 __________。 |
(2)探究二氧化碳的性质 | ①该实验过程中,可观察到的现象是____。 ②从实验现象得出,二氧化碳具有的性质是__。这一性质在实际生活中的应用为____。 |
(3)测定空气的成分(试管容40mL,白磷过量且白磷所占体积与导管内的气体体积忽略不计) | ①实验前,打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明:_____; ②若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹。可观察到的现象为___________________。 ③若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,试管冷却。可观察到的现象______________________________________________________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是两种固体的溶解度曲线。
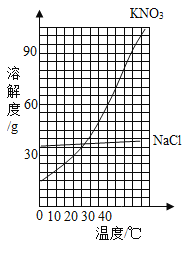
(1)40℃时,氯化钠的溶解度_________(填“>”、“=”或“<”)硝酸钾的溶解度。
(2)硝酸钾的溶解度随温度的升高而_____________。
(3)若将饱和的硝酸钾溶液从40℃降温到10℃,_____(填“有”或“无”)晶体析出。
(4)20℃时,某实验小组取不同质量的硝酸钾,分别加入到100g水中,充分溶解后,所得溶液的质量与加入硝酸钾的质量对应关系如表:
实验一 | 实验二 | 实验三 | 实验四 | |
硝酸钾的质量/g | 20.0 | 25.0 | 30.0 | 35.0 |
所得溶液的质量/g | 120.0 | 125.0 | 130.0 | 131.6 |
根据上表数据,实验二所得的溶液为__________(填“饱和”或“不饱和”)溶液;20℃时,硝酸钾的溶解度为_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)氧气是生产生活中重要的物质。
(1)氧气有很多用途。下列属于氧气用途的是 和 (填序号)。
A.医疗急救 B.食品防腐 C.航天火箭 D.霓虹灯
(2)氧气能跟很多物质反应。根据下图所示实验,并阅读资料,回答下列问题。

Ⅰ.小明对图1铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
①表中“未填”部分的内容应为__ ___;
②铁丝在氧气燃烧的文字表达式是___ 。
集气瓶底部放少量水或细沙的作用是______________________
③通过以上探究,你认为铁丝燃烧产生火星四射现象的原因可能是__ ____。
Ⅱ.图2中的反应现象为 ,反应的文字表达式为 ,集气瓶中加入的液体可能是 ,其主要目的是___ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F是初中化学常见的物质,都含有一种相同的元素。其中B是常见的溶剂,D和F是组成元素相同的气体,E是铁锈的主要成分。它们的相互关系如图所示(图中“﹣”表示两端的物质间能发生反应,“→”表示物质间存在转化关系;部分反应物、生成物和反应条件已略去)。请回答。
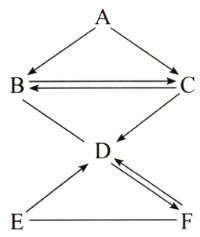
(1)B的化学式是_____。
(2)写出D的一种用途_____。
(3)E和F反应的化学方程式为_____。
(4)A→C化学反应的基本类型是_____反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】玲玲在学习复分解反应时,对复分解反应的条件产生了兴趣,于是她和小组内的同学仅用以下药品展开了探究活动。
实验药品:稀H2SO4、稀HCl、NaOH溶液、Na2CO3溶液、Ba(NO3)2溶液、NaCl溶液、酚酞溶液
(提出问题)复分解反应发生的条件是什么?
(查阅资料)硝酸钡溶液显中性,且Ba2+有毒。
(实验探究)玲玲用上述物质做了下列几组实验。
组合序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
组合物质 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 | H2SO4 Ba(NO3)2 | NaOH Ba(NO3)2 | Na2CO3 Ba(NO3)2 |
(记录和解释)(1)组合①、②、⑤均无明显现象,其中组合_____与另外两组的实质不同。为证明该不同之处,玲玲在实验过程中使用了酚酞溶液。
(2)请写出组合④的化学方程式_____________。
(实验结论)他们请教老师并讨论后知道,只有当两种化合物互相交换成分,生成物中有沉淀或水或气体生成时,复分解反应才可以发生。
(应用)写出利用熟石灰鉴别化肥氯化铵和氯化钾有关反应的化学方程式_______________________。
(拓展延伸)实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。
为了确定沉淀和清液的成分,继续展开探究。
(实验1)探究沉淀的成分。
(提出猜想)Ⅰ.沉淀只有BaSO4 Ⅱ.沉淀只有BaCO3 Ⅲ.沉淀中含有BaSO4和BaCO3。
梅梅取少量沉淀于试管中,滴加过量的______,观察到沉淀部分溶解,证明了猜想Ⅲ是正确的。
(实验2)探究清液的成分。
①取少量清液于试管中,向其中滴加几滴硝酸钡溶液,无明显现象。
②另取少量清液于另一只试管中,滴加几滴______________,有白色沉淀产生。
(解释与结论)探究活动结束后,小组内成员通过讨论分析,一致认为清液中含有的离子除Na+、Cl-外,还有____________________(指示剂除外)。
(处理废液)为了防止污染环境,玲玲向废液缸中加入适量的_________,对废液进行处理后,将固体回收进一步处理,溶液排放。
(交流与反思)根据你对物质溶解性的了解,结合复分解反应发生的条件,请写出一种在水溶液中一般不能发生复分解反应的可溶性盐_____________(写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废铁屑的主要成份是铁,同时还有少量铁锈(主要成分是Fe2O3)等杂质,动物饲料硫酸亚铁的生产工艺之一如下图所示:
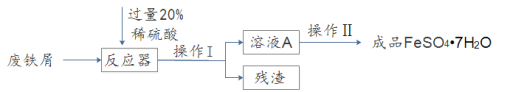
(1)实验室欲用98%的浓硫酸(密度为1.84g/ml)配制200g20%的稀硫酸,有以下实验步骤:a.量取;b.计算;c.稀释;d.装瓶贴标签。正确的顺序是__(填字母),若用量筒量取浓硫酸时俯视读数,其它操作正确,则所得溶液的质量分数___20%(填“>”、“<”或“=”)。
(2)在反应器中发生的化学反应①Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O;② Fe2(SO4)3 + Fe = 3FeSO4 ;③______。反应器所在的厂房要严禁烟火、加强通风的原因是________。
(3)溶液A中的溶质是______(填化学式)。
(4)操作Ⅰ的名称是_____,完成操作Ⅰ的玻璃仪器有:玻璃棒、烧杯和________,玻璃棒的作用_______。
(5)经过操作Ⅱ:____、降温结晶、过滤、冰水洗涤、低温干燥可得硫酸亚铁晶体(FeSO47H2O),用低温干燥说明硫酸亚铁晶体可能具有的性质是____。
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成Fe2O3 和SO2、SO3两种气体,试写出该反应的化学方程式________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取一定质量的CaCO3固体高温加热一段时间后,冷却,测得剩余固体的质量为8.0g,其中,钙元素质量分数为50.0%.下列判断正确的是( )
A. 生成2.0gCO2气体
B. 原来CaCO3的质量为14.5g
C. 剩余8.0g固体为纯净物
D. 剩余8.0g固体中加入稀盐酸无明显现象
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com