
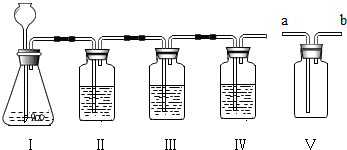
 在实验室中,同学们用如图装置制取纯净的CO2,下列说法正确的是( )
在实验室中,同学们用如图装置制取纯净的CO2,下列说法正确的是( )| A. | Ⅰ中固体反应物是大理石,液体反应物是稀H2SO4 | |
| B. | Ⅱ中液体是浓H2SO4,其作用是吸收CO2气体中混有的H2O | |
| C. | Ⅱ中的试剂是饱和碳酸氢钠溶液、Ⅲ中没有白色沉淀,说明CO2气体中已经不含HCl | |
| D. | 若用Ⅴ装置收集CO2气体,应从b端进气 |
分析 A、根据大理石和稀硫酸反应生成的硫酸钙是微溶于水的,覆盖在碳酸钙的表面,阻止了碳酸钙与稀硫酸的进一步接触,使反应停止去分析解答;
B、根据要得到纯净的二氧化碳,应先通过饱和碳酸氢钠溶液除去氯化氢气体,再干燥进行解答;
C、根据氯化氢气体溶于水形成盐酸,盐酸可以和硝酸银反应生成不溶于水的氯化银沉淀去分析解答;
D、根据二氧化碳的密度比空气大,应从长管进气进行分析解答.
解答 解:A、大理石和稀硫酸反应生成的硫酸钙是微溶于水的,覆盖在碳酸钙的表面,阻止了碳酸钙与稀硫酸的进一步接触,使反应停止,因此制取二氧化碳用盐酸,而非硫酸,故A错误;
B、要得到纯净的二氧化碳,应先通过饱和碳酸氢钠溶液除去氯化氢气体,再利用浓硫酸干燥,故Ⅱ中液体是饱和的碳酸氢钠溶液,用来吸收氯化氢气体,故B错误;
C、氯化氢气体溶于水形成盐酸,盐酸可以和硝酸银反应生成不溶于水的氯化银沉淀,由于Ⅲ中没有白色沉淀产生,则说明气体中已经不含有HCl气体,故C正确;
D、由于二氧化碳的密度比空气大,故应从长管进气,将空气挤压到集气瓶上部排出,故D错误;
故选:C.
点评 本题考查了实验室制取二氧化碳的原理、收集方法及除杂等,是中考的重点,应先除杂再检验是否除尽,然后干燥收集.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
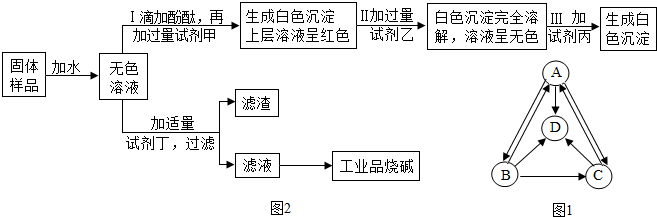
| 实验步骤 | 实验现象 |
| Ⅰ.向样品溶液中滴加酚酞溶液 | 溶液呈红色 |
| Ⅱ.向样品溶液中滴加稀硫酸, 并用玻璃棒搅拌 | 滴加一定量稀硫酸后溶液中开始产生气泡 溶液仍呈红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2012年4月15日,央视《每周质量报告》报道了部分药品生产企业使用铬超标胶囊生产药品的问题.铬虽然是人体必需的一种微量元素,但过量的摄入会对人体造成危害,影响人体的抗氧化系统,溶液得糖尿病、高血压、肿瘤等多种疾病.请回答下列问题:
2012年4月15日,央视《每周质量报告》报道了部分药品生产企业使用铬超标胶囊生产药品的问题.铬虽然是人体必需的一种微量元素,但过量的摄入会对人体造成危害,影响人体的抗氧化系统,溶液得糖尿病、高血压、肿瘤等多种疾病.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
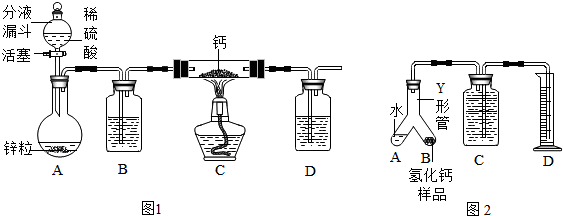
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
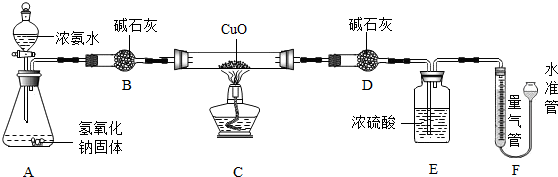
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com