
 某研究小组发现,维C泡腾片(主要成分如图所示)溶于水,有许多气泡产生,小组同学对该气体的成分进行了如下探究:
某研究小组发现,维C泡腾片(主要成分如图所示)溶于水,有许多气泡产生,小组同学对该气体的成分进行了如下探究:
【猜想与假设】
卓玛说:该气体可能是O2、H2、SO2、CO、CO2。
扎西说:不可能有SO2,因为 。
德吉说:不可能有H2和CO,从药品安全角度考虑,H2易燃易爆,CO 。
讨论后,小组同学认为该气体可能有O2、CO2中的一种或两种。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清石灰水中 | 澄清石灰水 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
【得出结论】
(1)由实验①可知,该气体中肯定含有  ,写出该反应的化学方程式:
,写出该反应的化学方程式:  。
。
(2)由实验②不能确定该气体中不含氧气,理由是 。
【拓展延伸】向维C泡沸片溶液中滚圆石蕊试液,溶液变红,说明溶液显 性。
科目:初中化学 来源: 题型:
某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是()

|
| A. | HCl和H2SO4一定存在 |
|
| B. | NaOH、H2SO4和MgCl2一定不存在 |
|
| C. | HCl和MgCl2一定存在 |
|
| D. | HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在 |
查看答案和解析>>
科目:初中化学 来源: 题型:
甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.

(1)若甲能供给呼吸,乙为无色液体,反应②的化学方程式为 ______ _________ ___ ,基本反应类型是 _____ ____ ;
(2)若甲、乙均是某非金属元素的气态氧化物,甲有毒,反应①的化学方程式为 _____ ___ ______ ______ _________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列选项中,除杂试剂或方法不正确的是( )
| 选项 | 物质 | 杂质 | 除杂试剂或方法 |
| A | KCl | MnO2 | 溶解、过滤、蒸 |
| B | NaCl | Na2CO3 | 加入适量稀硫酸、蒸发 |
| C | Cu | CuO | 加入足量稀盐酸、过滤 |
| D | CaO | CaCO3 | 高温煅烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:
图甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
 (1)t1℃时,甲、乙、丙的溶解度由大到小的顺序是 。
(1)t1℃时,甲、乙、丙的溶解度由大到小的顺序是 。
(2)P点的含义 。
(3) t3℃时,在150g水中加入100g甲,所得溶液 (选填“是”或“不是”)饱和溶液,形成溶液的质量为 g。
(4) t2℃时,甲、乙、丙三种物质的饱和溶液升温至t3℃后,三种溶液的溶质质量分数由大到小的顺序是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
酸性较弱的环境有利于益生菌生长,维持皮肤菌群平衡。因此淋浴液的酸碱度宜为( )。
A. pH<0 B. 4.5<pH<6.5
C. 8<pH<10 D. pH>14
查看答案和解析>>
科目:初中化学 来源: 题型:
下列三个实验均可证明CO2能与NaOH溶液反应。
实验Ⅰ:用试管集满CO2,迅速加入NaOH溶液、塞紧橡皮塞,充分振荡,静置。
(1)实验后打开橡皮塞时,听到响亮的“啵”声,其原因是实验后试管中的气压________(填“变大”或“变小”);
(2)对静置后的溶液进行下列操作,由对应的现象可推知CO2与NaOH溶液一定反应的是________(填序号)。
a. 滴加酚酞,溶液变为红色
b. 滴加少量稀盐酸,不产生气泡
c. 滴加少量氯化钡溶液,产生白色沉淀
实验Ⅱ:在8.0 g NaOH固体中加入适量95%的乙醇溶液,配制成饱和NaOH的乙醇溶液,向该溶液中通入CO2,直至产生白色沉淀Na2CO3。
(1)某托盘天平标尺的最大刻度为1 g,配备有1 g、2 g、5 g和10 g四种砝码若干个,用该天平称取8.0 g NaOH固体时,所需砝码总数为________个;
(2)实验Ⅱ利用的原理是:________影响物质的溶解性。
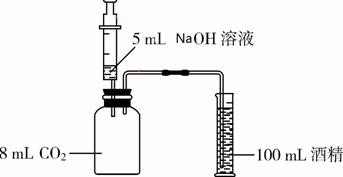
实验Ⅲ:如图5所示,将5 mL溶质质量分数为10%的NaOH溶液(ρ≈1.1 g/mL)缓慢、全部注射入瓶中,观察到酒精倒流入瓶中,最终瓶中剩余5 mL气体。此实验条件下,1体积水约可溶1体积CO2,CO2不溶于酒精,ρ(CO2)≈2 gL。
(1)实验时________(填“能”或“不能”)用水代替量筒中的酒精;
(2)实验时将NaOH溶液缓慢注射入瓶中的原因是________;
(3)根据上述实验可推知:与NaOH溶液反应的CO2约为________(取整数)mL;
(4)理论上,上述5 mL NaOH溶液与足量CO2反应都转化为Na2CO3时,参加反应的CO2的体积大约为多少毫升?(写出计算过程,结果取整数)
(5)实际上,上述NaOH溶液吸收的CO2偏少,其原因可能是________(填序号)。
a . CO2不纯 b. 装置漏气
. CO2不纯 b. 装置漏气
c. NaOH与CO2化合生成了NaHCO3
d. 倒流入瓶中的酒精干扰了NaOH溶液对CO2的吸收
查看答案和解析>>
科目:初中化学 来源: 题型:
黄铜矿(主要万分CuFeS2)经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4.某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜.主要步骤如图所示:
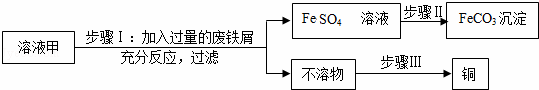
(1)Fe2(SO4)3与铁反应的化学方程式:xFe2(SO4)3+yFe=zFeSO4,其中x、y、z为化学计量数,z的值为 .
(2)步骤Ⅰ中,生成铜的化学方程式: .
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是 .
(4)步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可以是 (填化学式).
(5)步骤Ⅲ回收铜的方法为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com