
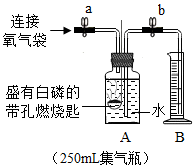
 研究性学习小组的同学们在实验室中对某种家用制氧机制出的气体进行研究.
研究性学习小组的同学们在实验室中对某种家用制氧机制出的气体进行研究.| 实验次序 | 1 | 2 | 3 | 4 | 5 |
| B中剩余水体积/mL | 100 | 41 | 38 | 42 | 39 |
分析 实验I:根据碳在氧气中燃烧生成了二氧化碳写出反应的化学方程式;
实验II:
[实验步骤]③根据白磷燃烧生成了五氧化二磷写出反应的化学方程式;
④根据氧气能与白磷反应分析;
[数据处理和分析]
(1)比较表中的数据,分析数据偏差较大的实验,根据实验的注意事项分析导致产生较大误差的可能原因;
(2)根据表中的数据计算气体中氧气的体积分数.
解答 解:实验I:碳与氧气反应生成二氧化碳,反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
实验II:
[实验步骤]③白磷与氧气在点燃条件下反应生成五氧化二磷,该反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
④若收集的氧气是纯氧,能全部与白磷反应,待白磷熄灭并冷却到室温,打开止水夹,观察到集气瓶中有剩余的气体的现象,说明收集的气体不是纯净的氧气.
[数据处理和分析]
(1)由上表数据可知,第1次数据偏差较大,导致产生较大误差的可能原因是实验时白磷不足等.
(2)200mL气体中氧气体积为:200mL-($\frac{41+38+42+39}{4}$)mL=160mL,
小丽所带气体中氧气的体积分数为:$\frac{160mL}{200mL}$×100%=80%.
故答为:实验I:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
实验II:
[实验步骤]③4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
④集气瓶中有剩余的气体.
[数据处理和分析]
(1)1,白磷不足等.
(2)80.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 步步高达标卷系列答案
步步高达标卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com