
 某研究性学习小组在研究由Fe2+制备Fe(OH)2:
某研究性学习小组在研究由Fe2+制备Fe(OH)2:| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
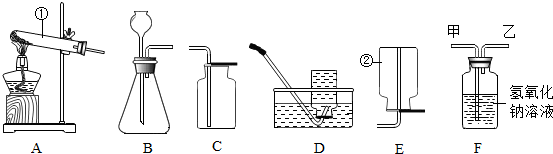
分析 (2)关闭活塞C,A瓶内铁粉与稀硫酸反应放出的氢气不能排出而使瓶内气体增加,压强逐渐增大,把反应生成的硫酸亚铁溶液压入B瓶内,氢氧化钠与硫酸亚铁发生反应而生成氢氧化亚铁的沉淀,因此,在B瓶内观察到沉淀产生;
(3)由资料信息可知,氢氧化亚铁为白色而氢氧化铁为棕色,二者的混合物呈现出绿色,因此实验中出现灰绿色或绿色的现象应是生成的Fe(OH)2部分被氧化而混入少量的Fe(OH)3的缘故;
(4)Fe (OH)2•nH2O受热分解生成氢氧化亚铁和水;
(5)合理设计实验,可以科学地解释由Fe2+制备Fe(OH)2的过程中,沉淀由“白”变“绿”的原因.
解答 解:(2)关闭活塞C,A瓶内铁粉与稀硫酸反应放出的氢气不能排出而使瓶内气体增加,压强逐渐增大,把反应生成的硫酸亚铁溶液压入B瓶内,氢氧化钠与硫酸亚铁发生反应而生成氢氧化亚铁的沉淀,因此,在B瓶内观察到沉淀产生;
铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑;
硫酸亚铁和氢氧化钠反应生成氢氧化亚铁沉淀和硫酸钠,反应的化学方程式为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;
为了防止生成的氢氧化亚铁被氧化,反应开始应该打开C,目的是利用产生的氢气,排出装置中的空气.
故填:B;Fe+H2SO4=FeSO4+H2↑;FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;利用产生的氢气,排出装置中的空气.
(3)上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,是由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3.
故填:由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3.
(4)用热水浴的方式加热生成的绿色沉淀,观察到沉淀由绿变白的趋势,说明Fe (OH)2•nH2O受热分解生成氢氧化亚铁和水,反应的化学方程式为:Fe(OH)2•nH2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)2+nH2O.
故填:Fe(OH)2•nH2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)2+nH2O.
(5)在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路可以是:向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者将Fe(OH)3和Fe(OH)2混合后观察其颜色).
故填:向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者将Fe(OH)3和Fe(OH)2混合后观察其颜色).
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 天天向上口算本系列答案
天天向上口算本系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 物质在空气中燃烧的反应都是化合反应 | |
| B. | 自然界中的碳循环主要是通过化学变化来实现 | |
| C. | 氧化物就是含氧元素的化合物 | |
| D. | 可燃物在空气中不一定能燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用Al(OH)3治疗胃酸过多症 | |
| B. | 用稀盐酸除去炭粉中的CuO | |
| C. | 用适量BaCl2溶液除去K2SO4溶液中的KOH | |
| D. | 实验室用在H2O中加少量NaOH以增强水的导电性来电解水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com