
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
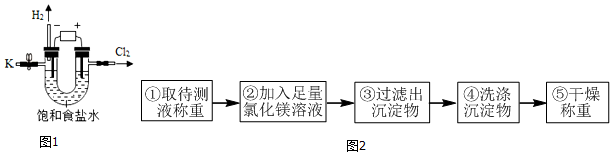
分析 (1)电解饱和食盐水生成烧碱、氢气和氯气,书写对应的化学方程式即可.
(2)酚酞遇碱变红;
(3)根据实验方法进行方案的分析与评价.
(4)根据恰好完全反应所用的盐酸的量和对应的化学方程式计算.
解答 解:(1)电解饱和食盐水生成烧碱、氢气和氯气,该反应的化学方程式为 2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)为了检验待测液中含有氢氧化钠,某同学取待测液滴加酚酞溶液,由于酚酞遇碱变红,而题目给出的结论是含有氢氧化钠,所以对应的现象是出现红色.
(3)为了测定待测液中氢氧化钠的质量分数,可以用沉淀法.沉淀法是将氢氧化钠转化为沉淀,然后通过沉淀的质量计算氢氧化钠的质量.
a.步骤②须加入足量的氯化镁溶液,加入氯化镁是因为氯化镁和氢氧化钠能反应生成氢氧化镁沉淀,加入足量是使氢氧化钠完全转化,所以加入足量的氯化镁溶液的目的是 将氢氧化钠全部转化为氢氧化镁,发生反应的化学方程式为 2NaOH+MgCl2=Mg(OH)2↓+2NaCl.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的,也就是判断是否有剩余的氢氧化钠,此时需要静置后取上层清液于试管中,滴加氯化镁溶液,若观察到无明显现象,则证明氯化镁溶液已经足量.
b.利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,导致氢氧化镁表面有杂质,也就是氢氧化镁的质量偏大,对应的氢氧化钠也就偏大,所以所计算的氢氧化钠的质量分数将 偏大.
(4)由表中数据可知,加入9.8g稀盐酸时恰好完全反应,此时消耗的HCl的质量为1.02g/mL×9.8mL×7.3%≈0.73g
设氢氧化钠的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 0.73g
$\frac{40}{36.5}$=$\frac{x}{0.73g}$
x=0.8g
待测液中氢氧化钠的质量分数为$\frac{0.8g}{4g}$×100%=20%
答案为:
(1)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)红色.
(3)a. 将氢氧化钠全部转化为氢氧化镁,2NaOH+MgCl2=Mg(OH)2↓+2NaCl. 氯化镁; 无明显现象.b. 偏大.
(4)20%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
| A. | 在溶液中K+和SO42-能大量共存 | |
| B. | 氯化钠是由氯化钠分子构成的 | |
| C. | 最外层电子数决定了元素的化学性质 | |
| D. | 木炭还原氧化铜反应中,氧化铜是氧化剂,木炭是还原剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | A+2B=2C+D | B. | 2A+B=C+2D | C. | A+2B=C+2D | D. | 2A+B=2C+D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
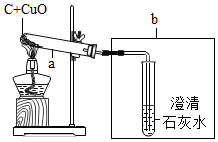 某化学兴趣小组的同学探究木炭还原氧化铜的实验,实验装置如图.实验时,a中的固体由黑色变红色,b中的试管内产生气泡和白色沉淀.
某化学兴趣小组的同学探究木炭还原氧化铜的实验,实验装置如图.实验时,a中的固体由黑色变红色,b中的试管内产生气泡和白色沉淀.
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  除去CO中的CO2 除去CO中的CO2 | B. | 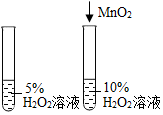 探究二氧化锰对反应速率的影响 | ||
| C. |  探究空气中氧气的含量 探究空气中氧气的含量 | D. |  探究影响物质溶解性的因素 探究影响物质溶解性的因素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
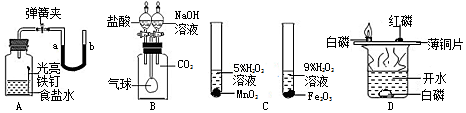
| A. | 证明铁生锈有空气参与 | B. | 确认CO2和 NaOH 已发生反应 | ||
| C. | 比较 MnO2 和 Fe2O3 的催化效果 | D. | 探究可燃物燃烧的条件 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com