
| A. | 铁在氧气中燃烧:2Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 硫酸铵与烧碱混合:( NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑ | |
| C. | 铝片放入硝酸银溶液中:Al+AgNO3═AlNO3+Ag | |
| D. | 向氯化镁溶液中滴入硫酸钾溶液:MgCl2+K2SO4═MgSO4↓+2KCl |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:A、生成物错误,生成物应是四氧化三铁,正确的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
B、化学方程式书写完全正确;
C、生成物硝酸铝化学式书写错误,正确的化学方程式为:Al+3AgNO3═Al(NO3)3+3Ag.
D、硫酸镁不是沉淀,该反应不能发生;
故选:B
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.


科目:初中化学 来源: 题型:填空题
 如图是a、b、c三种物质的溶解度曲线.
如图是a、b、c三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 表示分子个数的是③ | |
| B. | 表示离子所带电荷数的是② | |
| C. | 表示原子个数的是④ | |
| D. | 表示一个分子中含有某种原子个数的是① |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
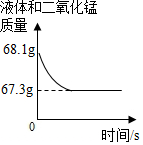 化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢质量分数.称量 68g 过氧化氢溶液和 0.1g 二氧化锰进行实验,反应前后质量随时间变化关系如图.计算:
化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢质量分数.称量 68g 过氧化氢溶液和 0.1g 二氧化锰进行实验,反应前后质量随时间变化关系如图.计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油锅着火后向锅中放入菜叶目的是降低油的着火点 | |
| B. | 家用煤加工成蜂窝煤是为了增大煤与氧气的接触面积 | |
| C. | 高层建筑物起火立即乘电梯撤离 | |
| D. | 不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 臭氧和氧气的化学性质不同 | B. | 臭氧是空气质量指数的污染物之一 | ||
| C. | 大量汽车尾气排放会导致臭氧污染 | D. | 佩戴口罩能有效阻挡臭氧的吸入 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度(℃) | 20 | 40 | 50 | |
| 溶解度/g | NaCl | 36.0 | 36.6 | 37.0 |
| KNO3 | 31.6 | 63.9 | 85.5 | |
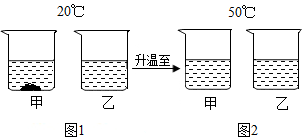
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com