

| A、此法的优点之一是原料来源丰富 | ||||
B、步骤①中发生的化学方程式为CaCO3
| ||||
| C、以上提取镁的过程,没有涉及反应类型的是置换反应 | ||||
| D、电解MgCl2与电解水一样分阴、阳极,电解时在阴极产生氯气 |


科目:初中化学 来源: 题型:
| 盐酸 |
| ||
| 熔融 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 MgCl2溶液
MgCl2溶液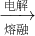 Mg+Cl2
Mg+Cl2查看答案和解析>>
科目:初中化学 来源:1993年第三届“天原杯”全国初中学生化学素质和实验能力竞赛复赛试卷(解析版) 题型:填空题
 MgCl2溶液
MgCl2溶液 Mg+Cl2
Mg+Cl2查看答案和解析>>
科目:初中化学 来源:2011年江苏省南通市海门市中考化学二模试卷(解析版) 题型:选择题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com