
【题目】由于二氧化碳与氢氧化钠反应无明显现象,对此同学们展开了探究,请你参与.
【提出问题】二氧化碳与氢氧化钠能否发生反应?
【查阅资料】常温下,氢氧化钠、碳酸钠在乙醇中的溶解性如下.
溶剂 | 乙醇 | |
溶质 | 氢氧化钠 | 碳酸钠 |
溶解性 | 易溶 | 难溶 |
【方案设计】小明同学设计了如图所示装置进行探究。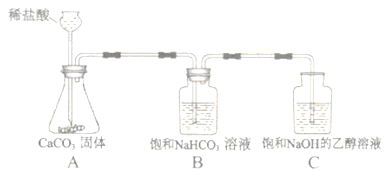
【实验探究】
(1)溶液配制.甲溶液:将一定质量的氢氧化钠固体加入到一定体积的乙醇中,用玻璃棒不断搅拌,使其成为饱和氢氧化钠的乙醇溶液.量取一定体积的乙醇要用到的仪器是 ,用玻璃棒搅拌的目的是 。
乙溶液:将一定质量的氢氧化钠固体加入到一定体积的75%的乙醇溶液中,用玻璃棒不断搅拌,使其成为不饱和氢氧化钠的乙醇溶液.判断甲、乙溶液形成的现象是 。
(2)进行实验,按图所示装置加入药品后进行实验.A中发生反应的化学方程式为 ,B装置的作用是 ,C中观察到的现象是 。
【实验结论】
(3)由此小明得出二氧化碳与氢氧化钠发生了化学反应,反应的化学方程式为 。
【反思交流】
(4)小刚同学认为小明的实验还足以证明二氧化碳与氢氧化钠发生了化学反应,还应补充的实验是 。
(5)若将图C中甲溶液换成乙溶液进行实验,C中可能无明显现象发生,原因可能是 。
【答案】(1)量筒和胶头滴管;加速溶解
(2)2HCl+CaCO3=CaCl2+H2O+CO2 ↑;除去氯化氢;溶液变浑浊
(3)2NaOH+CO2=Na2CO3+H2O
(4)将二氧化碳通入乙醇溶液,观察现象(5)碳酸钠易溶于水
【解析】
试题分析:量取一定体积的乙醇,因为乙醇是液体所以要用到的仪器是量筒和胶头滴管;用玻璃棒搅拌的目的是加速溶解,因为甲是饱和溶液而乙是不饱和溶液所以判断甲、乙溶液形成的现象是甲烧杯底部有固体,乙烧杯底部没有固体;A中发生反应的化学方程式为2HCl+CaCO3=CaCl2+H2O+CO2 ↑;B装置的作用是除去氯化氢气体;氢氧化钠和二氧化碳生成碳酸钠,碳酸钠难溶于乙醇,所以C中观察到的现象是溶液变浑浊,二氧化碳与氢氧化钠发生了化学反应,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O;小明的实验还足以证明二氧化碳与氢氧化钠发生了化学反应,还应补充的实验是将二氧化碳通入乙醇溶液,观察现象,防止是二者发生反应产生沉淀;将图C中甲溶液换成乙溶液进行实验,C中可能无明显现象发生,原因可能是碳酸钠易溶于水中,因为75%的乙醇溶液中含有水。


科目:初中化学 来源: 题型:
【题目】实验室中常需要使用硫酸。
(1)用小木棍蘸取少量浓硫酸,放置一会儿后,可观察到 。
(2)用温度计的液泡蘸取少量浓硫酸,放置在空气中一会儿,可观察到温度计显示温度升高,其原因是 。
(3)如果不慎将浓硫酸沾到皮肤上,应立即用 ,然后涂上3%~5%的碳酸氢钠溶液。
(4)实验室用98%的浓硫酸(密度1.84g/cm3)配制100g溶质质量分数为20%的稀硫酸。

①配制该溶液的步骤:计算、 、溶解(混匀)、装瓶贴标签;
②浓硫酸稀释过程如图所示,b中盛放的物质是 , a的作用是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】盐城濒临黄海,海盐文化全国知名.某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究:
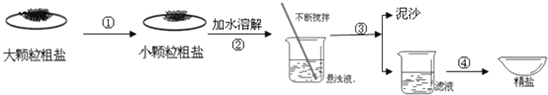
(1)操作①中必须用到的一种仪器是 (填序号)
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作③的名称是 ,操作④中用到玻璃棒,作用为 .
(3)用提纯得到的“精盐”配制100g 7.5%的氯化钠溶液.经检测,溶质质量分数偏小,其原因可能有 (填序号)
①氯化钠固体不纯
②称量时精盐与砝码放反了
③量取水时俯视读数
④装瓶时,有少量溶液洒出
(4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如下处理:

①白色沉淀的化学式为 .
②在得到的滤液中加入足量的稀盐酸的目的是 .
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将 (填“大于”、“小于”或“等于”)原精盐中NaCl的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:
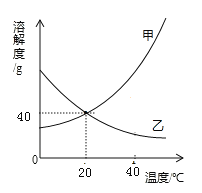
【题目】物质甲、乙的溶解度随温度变化图象如图所示,根据如图回答问题:
(1)由图你能获得哪些信息
① ;② 。
(2)20℃时,将50克甲溶于100克水中,所得溶液为 溶液(填“饱和”、“不饱和”溶液)。
(3)40℃时,甲、乙两种物质的溶解度大小关系:甲 乙(填“>”、“<”或“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】建立基本的化学观念可以让我们更好的理解化学,如形成守恒观念,可以更好的理解质量守恒定律,下列表述正确的是
A.每1个C原子和1个O2分子反应,生成2个CO2分子
B.32g S与32g O2完全反应,生成64g SO2
C.镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律
D.根据:蜡烛+氧气![]() 二氧化碳+水,则蜡烛中一定含有C、H、O三种元素
二氧化碳+水,则蜡烛中一定含有C、H、O三种元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活密切联系,生活中处处有化学.请你根据所学化学知识回答下列问题:
(1)从分子的角度解释,“酒‘香’不怕巷子深”的原因是 。
(2)在焙制糕点时常需加入一种名为“泡打粉”的膨松剂,其主要成分是NaHCO3,俗称 。
(3)淀粉发酵后可生产乙醇(C2H5OH),乙醇是一种清洁能源,其燃烧的化学方程式为: 。
(4)吸烟有害健康,烟草燃烧时产生的烟气中含有一种能与血红蛋白结合的有毒气体,它是 (填化学式)。
(5)在轿车的车箱内放入几包活性炭便可减少其中的异味,其原理是利用了活性炭的 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的第二杀手﹣﹣心脑血管疾病,这类疾病患者大多数属于酸性体质,应经常食用碱性食品.根据下表的信息,这类患者应经常食用的食物为( )
食物 | 葡萄 | 牛奶 | 豆制品 | 苹果 |
pH | 3.5~4.5 | 6.3~7.3 | 7.4~7.9 | 2.9~3.3 |
A.牛奶 B.葡萄 C.苹果 D.豆制品
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室利用如图装置进行组合,制取并收集氧气。
(1)写出标注仪器的名称:a ,b
(2)若选择①与⑤组合制取并收集氧气,反应的化学方程式是 ,实验结束时,应先 ,再停止加热.
(3)制取并收集干燥的氧气,下列组合可行的是 (填选项,可多选).
A.①③④ B.②③④ C.①③⑤ D.②③⑤
(4)选择装置②制氧气,分液漏斗盛装的药品是 过氧化氢溶液 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2015年3月18日,中科院院士谢毅教授凭借发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得第17届“世界杰出女科学家成就奖”。Ca2S3(硫化镓)是制作二维超薄半导体的材料之一。图Ⅰ、图Ⅱ分别是硫元素和镓元素在元素周期表中的信息,图Ⅲ分别是硫原子的原子结构示意图。
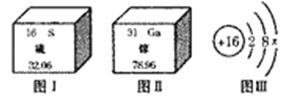
(1)图Ⅲ中x的数值为 ,镓元素的相对原子质量是 。
(2)用化学符号和数字表示:4个镓原子 ;2个硫离子 。
(3)硫化镓属于 (选填“单质”、“化合物”或“混合物”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com