
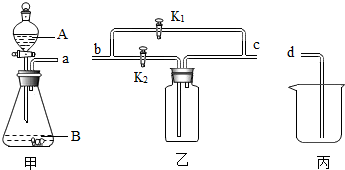
分析 (1)根据物质燃烧需要同时具备三个条件,即物质具有可燃性、与氧气接触、温度达到可燃物的着火点来分析解答;
(2)整个操作流程是:甲用来制取CO2,CO2制取出来后用碳酸氢钠溶液来吸收HCl,然后用来收集纯净的二氧化碳,结合化学反应来分析物质的质量.
解答 解:(1)①步骤1:丙中白磷的温度没有达到了着火点,并且没有与氧气接触,所以没有发生燃烧;故填:没有与氧气接触,且温度未达到白磷的着火点;
②步骤3:使乙中白磷燃烧的操作是打开K2,关闭K1,甲中产生的氧气进入乙中,由于乙的温度为80℃,故白磷燃烧;故填:打开K2,关闭K1;
(2)①若通入二氧化碳排出碳酸氢钠溶液,则气体应从短管进入,液体从短管排出,并连接d;故填:a→c→b→d;
②碳酸钠与系硫酸反应生成硫酸钠、水和二氧化碳,导致装置乙内压强增大,其中的液体被压入装置丙中,进入的丙中的液体体积即为生成二氧化碳的气体;故填:甲中有气泡产生,乙中的液体被排到丙中;
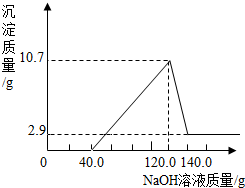
③部分变质的氢氧化钠中有碳酸钠和氢氧化钠两种物质,氢氧化钠与稀硫酸反应没有气体生成,碳酸钠与硫酸反应生成了二氧化碳,体积为V1;
5g的Na2CO3固体,重复上述操作,最终测得丙中液体体积为V2.且V2=5V1;由Na2CO3+H2SO4=Na2SO4+H2O+CO2↑可知,5g变质的NaOH固体样品中含碳酸钠的质量为1g,含氢氧化钠的质量为4g;故答案为:4.
点评 本题考查的比较全面,既考查了实验步骤的确定,又考查了数据的处理和有关的计算,综合性比较强,但只要认真分析,问题就不难解决.解答本题要根据燃烧的条件来分析.


科目:初中化学 来源: 题型:选择题
| A. | 碱溶液一定呈碱性,呈碱性的溶液不一定是碱溶液 | |
| B. | 置换反应一定有单质生成,有单质生成的反应不一定是置换反应 | |
| C. | 氧化物中一定含氧元素,含氧元素的化合物一定是氧化物 | |
| D. | 单质是只含一种元素的纯净物,含有一种元素的纯净物一定是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气可以用作食品保护气,是因为氮气化学性质活泼 | |
| B. | 洗洁精能洗去油污,是因为洗洁精对油污有乳化作用 | |
| C. | 自来水煮沸可以降低硬度,是因为加热时水中的部分钙、镁离子形成了沉淀 | |
| D. | 往锈蚀的锁芯内灌少量铅笔芯粉未易开锁,是因为铅笔芯中的石墨有润滑作用 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空.(1)汽车制造中用得最多的金属材料是钢.钢不是(填“是”或“不是”)纯金属.车体表面喷漆不仅美观,而且可有效防止钢铁与水和氧气接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空.(1)汽车制造中用得最多的金属材料是钢.钢不是(填“是”或“不是”)纯金属.车体表面喷漆不仅美观,而且可有效防止钢铁与水和氧气接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
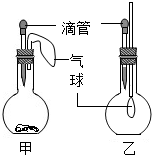 甲乙两位学生设计的实验如图所示.甲同学在烧瓶底部放入适量金属镁,乙同学在烧瓶中充满二氧化碳气体,两位同学挤压滴管分别滴入不同液体,导致两个气球均变大.请分析乙同学烧瓶里气球变大的原因是二氧化碳与氢氧化钠反应,瓶内压强减小.所发生反应的化学方程式是CO2+2NaOH═Na2CO3+H2O.用手触摸甲同学实验的烧瓶温度明显升高,说明化学能转变成内能.
甲乙两位学生设计的实验如图所示.甲同学在烧瓶底部放入适量金属镁,乙同学在烧瓶中充满二氧化碳气体,两位同学挤压滴管分别滴入不同液体,导致两个气球均变大.请分析乙同学烧瓶里气球变大的原因是二氧化碳与氢氧化钠反应,瓶内压强减小.所发生反应的化学方程式是CO2+2NaOH═Na2CO3+H2O.用手触摸甲同学实验的烧瓶温度明显升高,说明化学能转变成内能.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com