
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水,充分搅拌 | 固体完全溶解,形成无色溶液 |  |
| 步骤2:取少量步骤1形成的溶液与试管中,再滴加过量BaCl2溶液,震荡,静置 | 产生白色沉淀 | 含有Na2CO3 |
| 步骤3:取少量步骤2试管中的上层溶液与另一支试管中,再滴加少量MgCI2溶液,震荡 | 无明显现象 | 不含NaOH |
| 步骤4:另取一支试管,加入少量步骤1形成的溶液,再加入少量MnO2,将带火星木条伸入试管中 | 溶液中有气泡产生,带火星木条复燃 | 含有H2O2 |
分析 (1)根据含磷洗涤剂的使用能使水体富营养化,产生水华现象进行分析;
(3)根据质量守恒定律的微观解释分析解答,化学反应前后元素的种类不变进行分析;
(4)根据氯化钡和碳酸钠反应会生成碳酸钡沉淀,氢氧化钠么氯化镁会生成氢氧化镁沉淀,二氧化锰能催化过氧化氢分解生成氧气进行分析.
解答 解:(1)含磷洗涤剂的使用能使水体富营养化,产生水华现象;
(3)根据质量守恒定律的微观解释分析解答,化学反应前后元素的种类不变;
(4)氯化钡和碳酸钠反应会生成碳酸钡沉淀,氢氧化钠么氯化镁会生成氢氧化镁沉淀,二氧化锰能催化过氧化氢分解生成氧气,所以
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水,充分搅拌 | 固体完全溶解,形成无色溶液 |  |
| 步骤2:取少量步骤1形成的溶液与试管中,再滴加过量氯化钡溶液,震荡,静置 | 产生白色沉淀 | 含有Na2CO3 |
| 步骤3:取少量步骤2试管中的上层溶液与另一支试管中,再滴加少量MgCI2溶液,震荡 | 无明显现象 | 不含氢氧化钠 |
| 步骤4:另取一支试管,加入少量步骤1形成的溶液,再加入少量二氧化锰,将带火星木条伸入试管中 | 溶液中有气泡产生,带火星的木条复燃 | 含有H2O2 |
| 实验步骤 | 实验现象 | 实验结论 |
| 过量氯化钡溶液 | 产生白色沉淀 | |
| 不含氢氧化钠 | ||
| 二氧化锰 | 溶液中有气泡产生,带火星的木条复燃 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
| 体液 | A、血液 | B、胃液 | C、唾液 | D、胆汁 |
| pH范围 | 7.35-7.45 | 0.8-1.5 | 6.6-7.1 | 6.8-7.4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使混合气体通过氢氧化钠溶液 | B. | 将混合气体点燃 | ||
| C. | 使混合气体通过灼热的氧化铜 | D. | 使混合气体通过灼热的焦炭 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH和NH4NO3 | B. | CuSO4和Na2SO4 | C. | Na2CO3和CaCO3 | D. | NaCl和KCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
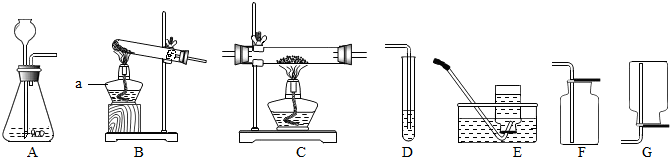
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
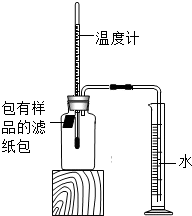 某实验小组对铁的锈蚀进行如下实验.室温时,将包有样品(足量)的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入广口瓶(容积150mL).当温度恢复至室温,且量筒内水面高度不变时读数.记录起始和最终量筒的读数以及所需时间,如表:
某实验小组对铁的锈蚀进行如下实验.室温时,将包有样品(足量)的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入广口瓶(容积150mL).当温度恢复至室温,且量筒内水面高度不变时读数.记录起始和最终量筒的读数以及所需时间,如表:| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
| ② | 1g铁粉、0.2g碳和10滴水和少量NaCl | 100 | 70 | 约70 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 可能出现的实验现象 | 实验结论 |
| (1)取少量滤液于试管中,加入Na2CO3溶液 | 产生白色沉淀 | 假设③成立 |
| (2)取少量的滤液于两支试管中分别加入碳酸钠溶液、稀盐酸 | 都无明显现象 | 假设①成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com