
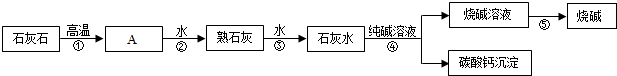
分析 (1)根据石灰石高温煅烧生成氧化钙和二氧化碳,物理变化是指没有新物质生成的变化,进行分析解答.
(2)分离烧碱溶液和碳酸钙混合物,即将不溶于水的固体与液体分离,进行分析解答.
(3)根据烧碱的用途,进行分析解答.
(4)根据石灰石高温煅烧生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
解答 解:(1)石灰石高温煅烧生成氧化钙和二氧化碳,A为氧化钙,能与水反应生成氢氧化钙,A可作为食品的干燥剂.
上述①-⑤四个步骤,分别是石灰石高温煅烧生成氧化钙和二氧化碳、氧化钙与水反应生成氢氧化钙,熟石灰溶于水、氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠、烧碱溶液蒸发得到烧碱,③⑤没有新物质生成,属于物理变化.
(2)第④步中,分离烧碱溶液和碳酸钙混合物时用到的操作名称叫过滤;第⑤步获得烧碱晶体的操作过程是加热浓缩、冷却、结晶.
(3)烧碱可用于造纸、制肥皂、印染等.
(4)石灰石高温煅烧生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,分别属于分解反应、化合反应、复分解反应,故没有涉及到基本反应类型是置换反应.
故答案为:(1)干燥;③⑤;(2)过滤;结晶;(3)造纸等;(4)置换反应.
点评 本题难度不大,理解以石灰石和纯碱为原料生产烧碱的主要流程,掌握盐、碱、生石灰的化学性质是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
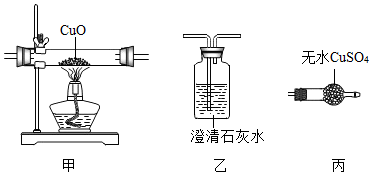 无水硫酸铜是白色固体,遇水变蓝,某气体可能含有水蒸气、CO、H2中的一种或几种,为确定成分,最佳的实验方案是将气体依次通入装置( )
无水硫酸铜是白色固体,遇水变蓝,某气体可能含有水蒸气、CO、H2中的一种或几种,为确定成分,最佳的实验方案是将气体依次通入装置( )| A. | 丙、甲.丙、乙 | B. | 丙、乙、甲、乙 | C. | 丙、甲、乙、丙 | D. | 甲、乙、丙、甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaSO4(BaCO3):加水,过滤 | |
| B. | Cu(CuO):过量稀盐酸,过滤 | |
| C. | NaCl溶液(Na2CO3):适量硝酸钙溶液,过滤 | |
| D. | CO(CO2):Fe2O3,高温 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
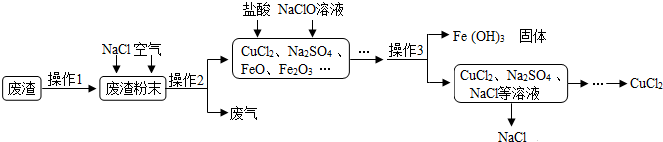
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
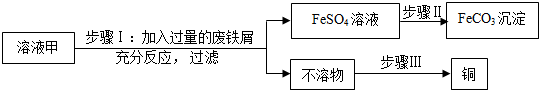
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
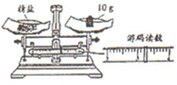 科学严谨的态度,安全规范的操作是成功进行化学实验的保障.
科学严谨的态度,安全规范的操作是成功进行化学实验的保障.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
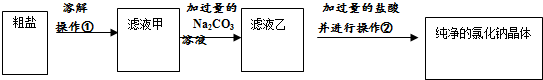
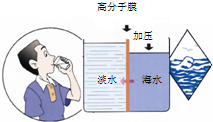
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
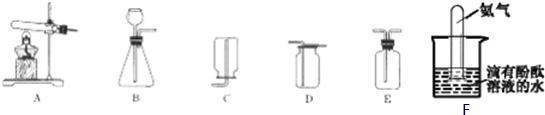
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
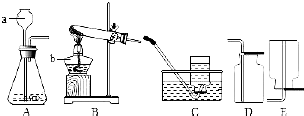 请根据如图所示实验装置回答问题:
请根据如图所示实验装置回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com