
分析 (1)物理性质是不经过化学变化就表现出来的性质,一般包括色态味、密度、熔沸点等性质;
(2)肼在常温下为液态;
(3)根据肼与助燃物质液态N2O4发生反应写出化学方程式;
(4)固体氢氧化钠具有吸水性,容易和空气中的二氧化碳发生化学反应;
(5)根据的性质进行分析
解答 解:(1)肼与氧化铁作用,易分解是经过化学变化才能表现出来的性质,属于化学性质;
(2)肼在常温下为液态;
(3)肼燃烧放热量大且燃烧产物对环境无污染,常用作火箭燃料,点燃时与助燃物质液态N2O4发生反应,生成N2和H2O.肼作为火箭燃料燃烧时反应的化学方程式为:2N2H4+N2O4$\frac{\underline{\;点燃\;}}{\;}$3N2↑+4H2O;
(4)固体氢氧化钠具有吸水性,容易和空气中的二氧化碳发生化学反应;
(5)因为肼有强烈的吸水性;能吸收空气中的二氧化碳;长期暴露在空气中易分解,所以肼需要密封保存;
故答案为:(1)AC;(2)液态;(3)2N2H4+N2O4$\frac{\underline{\;点燃\;}}{\;}$3N2↑+4H2O;(4)C;(5)有强烈的吸水性;能吸收空气中的二氧化碳;长期暴露在空气中易分解.
点评 此题主要考查肼的性质及应用,难度不大,所以要求同学们在平时的学习中加强知识的记忆.


科目:初中化学 来源: 题型:选择题
| A. | 某些金属的燃烧不能用CO2灭火 | |
| B. | 该反应是放出热量 | |
| C. | 该反应的实质是Mg和CO2中混有的O2反应 | |
| D. | 某些金属的燃烧不能用水扑救 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
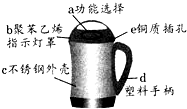 如图是家用豆浆机的功能结构示意图,请根据图回答下列问题:
如图是家用豆浆机的功能结构示意图,请根据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
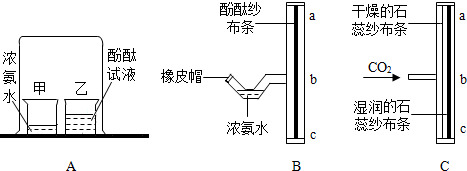
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 芹菜、动物肝脏、豆类中含有人体所需的铁元素 | |
| B. | 霉变食物中的黄曲霉毒素能损害人的肝脏,诱发肝癌等疾病 | |
| C. | 甲醛、一氧化碳、重金属中毒的原因都是它们与蛋白质反应,使其变质 | |
| D. | 铁、铜、氟、锡、铝都是人体必需的微量元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
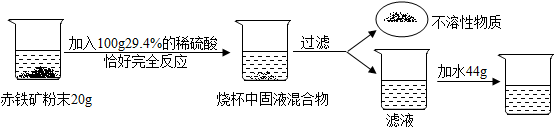
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com