11.空气中的SO
2含量和可吸入颗粒的含量(可用g/cm
3表示)都是重要的空气质量指标.在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02mg/L.
(1)为测定某地方的空气中SO
2和可吸入颗粒的含量,查阅资料得知:可用含有一定量碘的溶液测定空气中的SO
2含量,反应方程式是:SO
2+I
2+2H
2O═H
2SO
4+2HI.甲同学设计了如图1所示的实验装置:
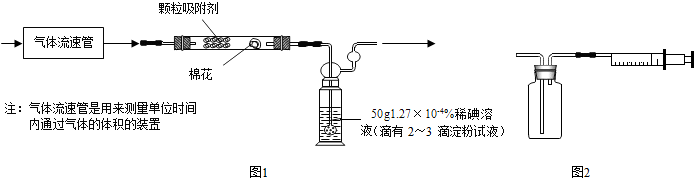
①应用上述装置测定空气中的SO
2含量和可吸入颗粒的含量,除测定气体流速(单位:cm
3/min)外,还需要测定溶液蓝色恰好褪去所需的时间 和吸收前后颗粒吸附剂、棉花、盛放容器的总质量.
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度.
请你协助甲同学完成稀碘溶液的配制:
第一步:准确称取1.27g碘单质加入烧杯中,同时加入少量碘化钾固体;
第二步:加适量水使之完全溶解,然后加水至溶液体积为1000mL;
第三步:从第二步所得溶液中,取出10.00mL溶液加入稀释至100mL.
(2)乙同学拟用下列简易装置测定空气中的SO
2含量:准确取50mL第三步所得的碘溶液,注入图2所示广口瓶中,加2~3滴淀粉指示剂,此时溶液呈蓝色.在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n).
①假设乙同学的测量是准确的,乙同学抽气的次数至少为800次,方可说明该地空气中的SO
2含量符合排放标准.
②如果乙同学用该方法测量空气中SO
2的含量时,所测得的数值比实际含量低,请你对其可能原因(假设溶液配制、称量或量取及各种读数均无错误)提出合理假设:抽气速度过快或_.
③丙同学认为:乙同学的实验方案需要抽气的次数太多,操作麻烦.与乙讨论后,决定只需抽气100次以下,即可说明空气中的SO
2含量符合排放标准.请你设计合理的改进方案:将50mL的碘溶液的体积减小为5mL,并将广口瓶改为试管.

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案