
| 反应前物质的质量/g | 反应后物质的质量/g | |
| 固体混合物 | 稀盐酸 | 蓝色滤液 |
| 4.0 | 未知质量 | 10.8 |
分析 (1)根据氧化铜和碳在高温的条件下生成铜和二氧化碳,铜不会与盐酸反应进行分析;
(2)根据盐酸和氧化铜反应的化学方程式和题中的数据进行计算.
解答 解:(1)氧化铜和碳在高温的条件下生成铜和二氧化碳,铜不会与盐酸反应,所以过滤所得滤渣中一定含有铜;
(2)依据质量守恒定律可知,参加反应的稀盐酸的质量为10.8g-x,
设固体混合物中氧化铜的质量为x
CuO+2HCl=CuCl2+H2O
80 73
x (10.8g-x)×7.3%
$\frac{80}{x}$=$\frac{73}{(10.8g-x)×7.3%}$
x=0.8g
故答案为:(1)铜;
(2)固体混合物中氧化铜的质量为0.8g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
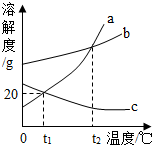 如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )| A. | t1℃时,50g水中最多能溶解10ga | |
| B. | 将t1℃时的c的饱和溶液升温,变为不饱和溶液 | |
| C. | a中含有少量b时,可以用降温结晶法提纯a | |
| D. | a、c的饱和溶液从t2℃降温到t1℃时,两种溶液的溶质质量分数:a>c |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体为氢气 |
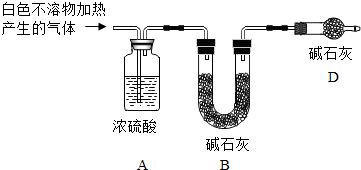
| 实验Ⅲ | ①取实验Ⅰ中少量的白色悬浊液,过滤,洗涤干净沉淀,然后稀盐酸 | ②产生气泡,沉淀全部溶解 | 白色不溶物含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 有白色沉淀产生 | ③澄清液中一定含有的溶质是Na2CO3(化学式) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 图中的反应物都是单质 | |
| B. | 该反应的化学方程式是 H2O+C$\frac{\underline{\;高温\;}}{\;}$CO+H2 | |
| C. | 该反应中原子的种类和数目均不变 | |
| D. | 化学反应前后碳元素化合价发生改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com