
 | 石蕊试液 | 氯化钡溶液 |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
分析 根据物质的性质、质量守恒定律的微观实质、化合价规则以及物质间反应的实验现象进行分析解答即可.
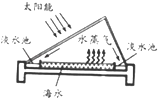
解答 解:(1)如图方法获得淡水是水的蒸发获取的,发生的是物理变化,故填:物理;
(2)2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,反应前含有12个Fe原子,16个H原子,16个O原子,6个Cl原子,反应后含有6个K原子,16个H原子,16个O原子,故6X中含有6个K原子,6个C磷原子,故X的化学式为KCl,K2FeO4中钾元素的化合价为+1,O元素的化合价为-2,设Fe元素的化合价为x,则有:(+1)×2+x+(-2)×4=0.x=+6,故填:KCl,+6.
(3)
 | 石蕊试液 | 氯化钡溶液 |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
点评 本题考查的是质量守恒定律的应用以及物质成分的推断,完成此题,可以依据已有的知识进行.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:解答题
 某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验:
某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质质量 | 田 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
| A. | 该反应是化合反应 | |
| B. | 在该反应中,丙物质一定做催化剂 | |
| C. | x=9g | |
| D. | 在该反应的化学方程式中,丙、丁的化学计量数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有C元素 | B. | 只有C、H元素 | C. | 含有C、H、O元素 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 称 量 项 目 | 质量(g) |
| NaOH和Na2CO3的混合物 | 9.30 |
| 锥形瓶+稀盐酸质量(过量) | 141.20 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合后,第一次称量的质量 | 148.50 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合后,第二次称量的质量 | 148.30 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合后,第三次称量的质量 | 148.30 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com