
| A. | 溶液甲可能是饱和溶液 | |
| B. | 溶液乙和溶液丙中的溶质质量分数可能相等 | |
| C. | 溶液乙一定是饱和溶液 | |
| D. | 溶液丙若再蒸发5g水,析出的晶体一定小于2g |
分析 饱和溶液是指在一定温度下一定量的溶剂中不能继续溶解某种溶质的溶液,若溶液中有未溶解的溶质存在,就说明这种溶液在该温度下是饱和的;同温度下的同物质的饱和溶液中溶质的质量分数相等.
解答 解:A、由于溶液甲蒸发掉5g水后,没有晶体析出,说明溶液甲是不饱和溶液,故A错误;
B、由于溶液乙蒸发掉5g水后,析出了2g晶体,则溶液丙一定是饱和溶液,如果乙溶液也是饱和的,则溶液乙和溶液丙中的溶质质量分数相等,故B正确;
C、由于溶液乙中不存在未溶解的溶质,因此乙溶液可能是饱和溶液也可能是不饱和溶液,故C错误;
D、由于乙溶液可能是不饱和溶液,而丙是饱和溶液,因此溶液丙若再蒸发5g水,析出的晶体可能大于2g,而乙溶液也是饱和,则丙是饱和溶液,因此溶液丙若再蒸发5g水,析出的晶体等于2g,故D不正确;
故选B.
点评 本题难度较大,主要考查了对饱和溶液和不饱和溶液的理解和应用.


科目:初中化学 来源: 题型:解答题
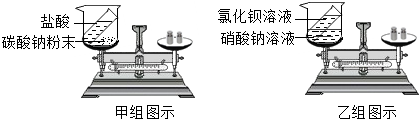
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸根中可能含有氧元素 | B. | 碱中一定含有金属元素 | ||
| C. | 碱中一定含有氢元素和氧元素 | D. | 酸中一定有非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 内壁有CaCO3的试管用稀盐酸清洗 | B. | 内壁有碘的试管用酒精清洗 | ||
| C. | 内壁有植物油的试管用洗洁精清洗 | D. | 内壁有铜粉的试管用稀硫酸清洗 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
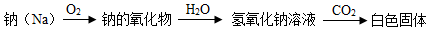
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和 NaOH |
| 2.过滤、取少量滤液加入无色酚酞试液 | 试液变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
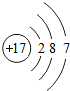 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com