解:(1)因为要检验二氧化碳的存在,所以要在A中盛放澄清的石灰水,因为二氧化碳能够使澄清的石灰水变浑浊;其中的氢气能够还原氧化铜,并生成水,所以要检验氢气的存在,要在D中盛放CuSO
4粉末,因为CuSO
4粉末遇水变蓝,可以用来检验有无水生成,就是检验氢气的存在.
故答案为:澄清石灰水;CuSO
4粉末;
(2)一氧化碳和氢气能够还原C中的氧化铜,化学反应式是:CuO+CO

Cu+CO
2,CuO+H
2
Cu+H
2O;一氧化碳还原氧化铜生成的二氧化碳气体能够与E中的石灰水反应生成碳酸钙沉淀和水.
故答案为:C:CuO+CO

Cu+CO
2,CuO+H
2
Cu+H
2O;
E:Ca(OH)
2+CO
2═CaCO
3↓+H
2O;
(3)为防止过量的一氧化碳污染空气,所以要进行尾气处理,因为CO具有可燃性,所以可进行燃烧处理.
故答案为:烧掉;
(4)B中盛放的物质浓H
2SO
4可以吸收水分,如果将A、B装置中药品对换,石灰水中的水分就会进入C装置,导致对管道煤气中是否含H
2的检验得不到准确结论,同时由于水蒸气的存在,将对C中的反应产生不良影响.
故答案为:A、B中药品交换后,进入C装置中的气体不干燥,导致对管道煤气中是否含H
2的检验得不到准确结论,同时由于水蒸气的存在,将对C中的反应产生不良影响.
分析:(1)根据要检验二氧化碳的存在分析A中应该盛放的物质;根据要检验氢气的存在分析D中应盛放的物质;
(2)根据一氧化碳和氢气能够还原C中的氧化铜分析C中发生化学反应的方程式;根据生成物中有二氧化碳存在分析E中发生反应的化学方程式;
(3)根据一氧化碳的可燃性处理尾气;
(4)根据B中盛放的物质浓H
2SO
4可以吸收水分分析.
点评:本题考查一氧化碳、二氧化碳、氢气的性质特点,以及相关的实验操作和化学反应式的书写,难度较大,同学们一定要慎重考虑.

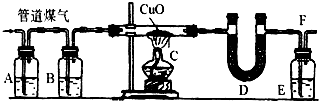 城镇居民烧水做饭用的管道煤气的主要成分是CO,其中也含有一定量的H2和少量CO2与水蒸气.为了验证其中H2、CO2的存在和管道煤气的还原性,某同学设计了如所示的实验装置.已知B中所盛物质为浓H2SO4、E中所盛物质为过量的澄清石灰水.其他所需的药品请从下列试剂中选择:浓H2SO4、CuSO4粉末、NaOH溶液、澄清的石灰水(若需要,药品可重复选用).
城镇居民烧水做饭用的管道煤气的主要成分是CO,其中也含有一定量的H2和少量CO2与水蒸气.为了验证其中H2、CO2的存在和管道煤气的还原性,某同学设计了如所示的实验装置.已知B中所盛物质为浓H2SO4、E中所盛物质为过量的澄清石灰水.其他所需的药品请从下列试剂中选择:浓H2SO4、CuSO4粉末、NaOH溶液、澄清的石灰水(若需要,药品可重复选用). Cu+CO2,CuO+H2
Cu+CO2,CuO+H2 Cu+H2O;一氧化碳还原氧化铜生成的二氧化碳气体能够与E中的石灰水反应生成碳酸钙沉淀和水.
Cu+H2O;一氧化碳还原氧化铜生成的二氧化碳气体能够与E中的石灰水反应生成碳酸钙沉淀和水. Cu+CO2,CuO+H2
Cu+CO2,CuO+H2 Cu+H2O;
Cu+H2O;

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案 城镇居民烧水做饭用的管道煤气的主要成分是CO,其中也含有一定量的H2和少量CO2与水蒸气.为了验证其中H2、CO2的存在和管道煤气的还原性,某同学设计了如所示的实验装置.已知B中所盛物质为浓H2SO4、E中所盛物质为过量的澄清石灰水.其他所需的药品请从下列试剂中选择:浓H2SO4、CuSO4粉末、NaOH溶液、澄清的石灰水(若需要,药品可重复选用).
城镇居民烧水做饭用的管道煤气的主要成分是CO,其中也含有一定量的H2和少量CO2与水蒸气.为了验证其中H2、CO2的存在和管道煤气的还原性,某同学设计了如所示的实验装置.已知B中所盛物质为浓H2SO4、E中所盛物质为过量的澄清石灰水.其他所需的药品请从下列试剂中选择:浓H2SO4、CuSO4粉末、NaOH溶液、澄清的石灰水(若需要,药品可重复选用).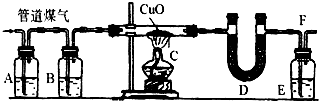
 Cu+H2O;E:Ca(OH)2+CO2═CaCO3↓+H2O
Cu+H2O;E:Ca(OH)2+CO2═CaCO3↓+H2O