
| A化学与安全 | B化学与生活 |
| 稀酸溅入眼睛--用大量水冲洗 进入地窖--先做灯火实验 | 服用氢氧化钠--治疗胃酸过多 人体需要适量补钙--防止患甲状腺疾病 |
| C化学与能源 | D化学与环保 |
| 化石燃料--煤、石油和天然气 清洁能源--太阳能、风能等 | 减少汽车尾气污染--提倡使用公共交通等 减少温室气体排放--利用水力、核能发电 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据灭火的原理以及二氧化碳不能供给呼吸和不燃烧也不支持燃烧进行解答;
B、胃酸过多即胃液酸性过强,治疗时应用碱性物质中和;
C、依据化石燃料的种类以及清洁能源的种类分析判断;
D、根据提倡使用公共交通可以减少汽车尾气污染以及开发并使用太阳能可以减少温室气体排放等进行解答.
解答 解:A、油锅着火可以用用锅盖盖灭;二氧化碳不能供给呼吸和不燃烧也不支持燃烧,进入地窖--先做灯火实验,故A正确;
B、氢氧化钠属于强碱,有强烈的腐蚀性,会腐蚀人的食管,不能服用氢氧化钠治疗胃酸过多症,故B错误;
C、三大化石燃料是煤、石油和天然气,它们的过度使用对环境质量下降影响较大,而太阳能、风能等使用时不会对环境造成危害,所以是相对清洁的能源,故C正确;
D、提倡使用公共交通可以减少汽车尾气污染,开发并使用太阳能可以减少温室气体排放,故D正确.
故选B.
点评 本考点综合性比较强,化学在生活中应用很广泛,因此要加强记忆有关的知识点,做题时要认真分析,综合把握.本考点经常出现在选择题和填空题中.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:初中化学 来源: 题型:解答题
| 锥形瓶+10.0g钙片+50.0g稀盐酸 | 次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 199.2 | 198.0 | 197.5 | 196.9 | 196.7 | 196.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
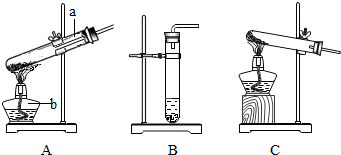
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 30 | 55 | 20 | 70 |
| 反应后的质量/g | 20 | 15 | X | 75 |
| A. | 该反应一定没有催化剂 | B. | 该反应一定是置换反应 | ||
| C. | X为45 | D. | 丁一定是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它是一种氧化物 | |
| B. | 组成中含有地壳中含量最多的金属元素 | |
| C. | 它是一种化合物 | |
| D. | K2FeO4中铁元素的化合价为+3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
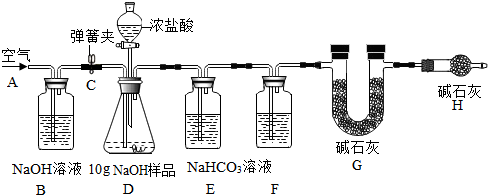
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
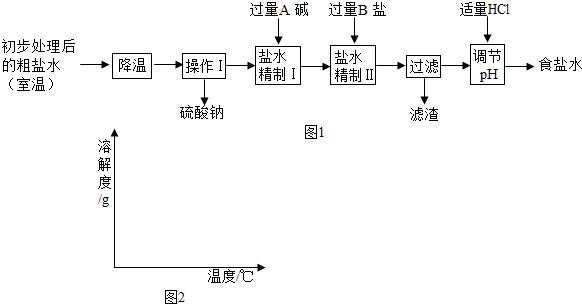
| 实验操作 | 实验现象 | 实验结论 |
| 温度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com