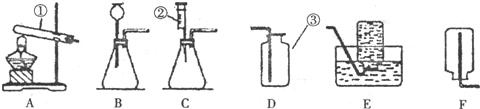
化学活动小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?
【猜想与假设】猜想1:在常温下能反应;
猜想2:在常温下不能反应,但在加热条件下能反应;
猜想3:在加热条件下也不能反应.
【实验与现象】实验1:将一小块铜片放入试管中,加入足量的浓硫酸,无明显现象;
实验2:加热该试管,铜片上有气泡生成,并闻到刺激性气味;
实验3:检验产生的有刺激性气味的气体;
实验4:立即停止加热;
实验5:将试管中的残液慢慢倒入少量水中,溶液呈蓝色.
【结论与解释】
(1)由以上探究可知猜想
2
2
是正确的(填序号)
(2)经检验产生的气体是SO
2,立即停止加热是为了避免产生更多的SO
2;
(3)铜跟浓硫酸在加热条件下反应后的产物只有SO
2和CuSO
4.
【反思与评价】探究结论中对产物是SO
2和CuSO
4的判断是否正确
不正确
不正确
,
理由
反应前后元素种类不同
反应前后元素种类不同
.
【拓展与应用】
根据以上探究和已掌握的知识,同学们设计了两个利用废铜屑、硫酸为原料制取硫酸铜的实验方案.
甲方案:利用废铜屑和浓硫酸在加热的条件下反应制取CuSO
4乙方案:在加热条件下将废铜屑在空气中氧化成CuO,再将CuO与稀硫酸反应制取CuSO
4请你从安全、节约、环保等方面进行评价,较好的方案是
乙方案
乙方案
,
理由是
不使用浓硫酸,安全
不使用浓硫酸,安全
.



 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案