
| �������������ˣ� | 19.50 |
| ����+̼���ƾ�����������ˣ� | 24.14 |
| ����+��ˮ̼���Ƶ��������ˣ� | 21.62 |
���� ���ݱ����е����ݣ����ǿ������̼���ƺ�ˮ������Ȼ����� Na2CO3•xH2O$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+xH2O���г�����ʽ�����ǾͿ��Լ����X�Ĵ�С��
��� �⣺������֪��̼���Ƶ�����Ϊ��21.62g-19.50g=2.12g
̼���ƾ����к��еĽᾧˮΪ��24.14g-21.62g=2.52g
Na2CO3•xH2O$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+xH2O
106 18x
2.12g 2.52g
$\frac{106}{2.12g}=\frac{18x}{2.52g}$
��ã�x=7
�𰸣�7��
���� �����Ĺؼ���Ѱ�ҹ�ϵʽ��ͬʱ���������ı仯ֵ��ʾ�ĺ��壮


 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
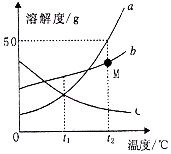 ��ͼ��a��b��c���ֹ������ʣ��������ᾧˮ�����ܽ������
��ͼ��a��b��c���ֹ������ʣ��������ᾧˮ�����ܽ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH+HCl�TNaCl+H2O | B�� | Zn+H2SO4�TZnSO4+H2 | ||
| C�� | H2O2�TH2��+O2�� | D�� | BaCl2+2KOH�T2KCl+Ba��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� �� | A | B | C | D |
| ��Ӧǰ������g�� | 19.7 | 8.7 | 31.6 | O.4 |
| ��Ӧ��������g�� | ���� | 17.4 | 0 | 3.6 |
| A�� | ����cһ���ǻ��������D�����ǵ��� | |
| B�� | ��Ӧ���ܱ�������A������Ϊ19.7g | |
| C�� | ��Ӧ�����У�����B������D�仯��������Ϊ87��36 | |
| D�� | ����A������C����Է�������֮��Ϊ197��316 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4•3H2O | B�� | CH4•5H2O | C�� | CH4•7H2O | D�� | CH4•8H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ��ʯ�͵��� | B�� | �����Ϳ��� | C�� | ���ۺ�ľ̿�� | D�� | �ƾ��Ͱ״� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʹ��һ������� | B�� | �����ӡ������������ļ� | ||
| C�� | ��Ļʽ����ȼ�ձ��� | D�� | ������ɫ���ÿλ��������ֲ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com