
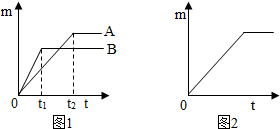
分析 (一)(1)根据金属活动性顺序的记忆情况填写即可;
(2)可从反应速率和氢气生成量两的方面来判断,镁、锌的反应速率要比铁快,由关系式计算可知m克铁生成m/28克氢气,m克锌可生成m/32克氢气,m克镁可生成m/12克氢气,镁反应最快生成氢气最多;锌反应比铁快生成氢气最少;铁反反应最慢生成氢气量居中;
(3)B线对应的金属为Zn那么A线比B线反应慢,生成氢气质量比锌多应为铁,从可写化学方程式;
(二)反应物种类相同时反应物浓度高反应速率快,20%的盐酸比5%的盐酸反应速率快;
(三)温度、反应物浓度、催化剂、反应物接触面积等都会影响化学反应速率,要研究一种条件对化学反应的影响,就要保持其它条件不变.
解答 解:(一)(1)根据金属活动性顺序可填:Mg、Al、Zn、Fe.
(2)A是活泼性较弱的金属,如果是铁,则B是锌时正好符合图中信息.故填:Zn.
(3)铁与稀盐酸反应生成氯化亚铁和氢气,故填:Fe+2HCl=FeCl2+H2↑
(二)反应物种类相同时反应物浓度高反应速率快,20%的盐酸比5%的盐酸反应速率快,且由于反应中所取锌片质量相同,所以生成的氢气质量相同,容易画出曲线如图: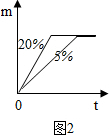
(三)温度、反应物浓度、催化剂、反应物接触面积等都会影响化学反应速率,要研究一种条件对化学反应的影响,就要保持其它条件不变,故答案应为:相同、相同.
点评 本题主要考查了化学方程式的书写、图象的画法及其金属活动性顺序等方面的内容,可以依据已有的知识结合题干提供的信息进行.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2AlO3 | ||
| C. | CO2+Ca(OH)2═CaCO3↓+H2O | D. | CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
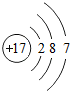 ,A元素在化学反应中容易得电子变成阴离子,属非金属元素(填“金属”或“非金属”);B元素的离子结构示意图为:
,A元素在化学反应中容易得电子变成阴离子,属非金属元素(填“金属”或“非金属”);B元素的离子结构示意图为: ,该离子带3个单位正电荷,该元素的原子核外总共有13个电子.A、B元素形成化合物的化学式(用A、B表示)为BA3.
,该离子带3个单位正电荷,该元素的原子核外总共有13个电子.A、B元素形成化合物的化学式(用A、B表示)为BA3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com