
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:
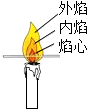 化学并不神秘,化学就在我们身边.只要我们采取适当的实验手段,留心观察,就能从司空见惯的事物中悟出很多科学道理.
化学并不神秘,化学就在我们身边.只要我们采取适当的实验手段,留心观察,就能从司空见惯的事物中悟出很多科学道理.查看答案和解析>>
科目:初中化学 来源: 题型:
| 氢气的性质 | 应用 |
| 用倒置在水槽中的装满水的瓶子收集氢气 | |
| 氢气被用于飞艇和载人气球 | |
| 人们用氦气代替氢气填充飞艇 | |
| 氢气用来制备金属钨 | |
| 氢气正在成为新兴的能源 |
| 催化剂 |
| 加热,加压 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、火上浇油:增加可燃物,使燃烧更剧烈 |
| B、釜底抽薪:将可燃物撤出燃烧区 |
| C、百炼成钢:逐渐降低生铁中碳、硅等含量 |
| D、花香四溢:说明分子可以再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| A、在点燃的条件下,氢气和氧气反应生成了水 |
| B、氢气加氧气反应生成水 |
| C、每4份质量的氢和32份质量的氧完全反应能生成36份质量的水 |
| D、在点燃的条件下,每二个氢气分子和一个氧分子化合生成二个水分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、化学反应发生时不一定能观察到明显的现象 |
| B、从物质的化学式可以判断物质中含有的元素 |
| C、配平化学方程式的依据是质量守恒定律 |
| D、一种元素只能组成一种单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 加入氢氧化钠溶液质量/g | 25 | 30 | 35 | 40 | 45 | 50 |
| 溶液颜色 | 红 | 红 | 红 | 紫 | 蓝 | 蓝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com