
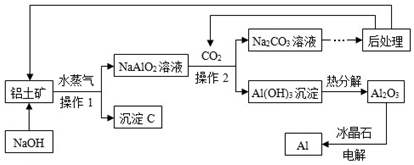
分析 (1)根据接触面积越大,反应越充分进行解答;
(2)根据题中的【查阅资料】部分进行解答;
(3)分析两个操作之后得到的物质进行解答;
(4)根据图中的信息可以完成解答;
(5)根据质量守恒定律进行解答;
(6)根据图中的信息可以知道NaAlO2溶液中通入CO2反应生成了碳酸钠和氢氧化铝,可以据此写出该反应的化学方程式.
解答 解:(1)铝土矿粉碎后接触面积增大,而接触面积越大,反应越充分;
(2)根据题中的【查阅资料】部分可以知道,氧化铁不能和氢氧化钠溶液反应,所以沉淀C为氧化铁,其化学式为:Fe2O3;
(3)分析两个操作之后得到的物质可以知道,操作后都得到了固体和液体,所以可以判断这两个操作为过滤,该过程中还需要漏斗等仪器;
(4)分析所给的过程可以知道,在此工艺中,氢氧化钠也是得到了循环利用,所以可循环使用的物质是CO2、H2O、NaOH;
(5)Al2O3是由铝元素和氧元素,所以电解Al2O3的化学方程式为:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑;
(6)根据图中的信息可以知道NaAlO2溶液中通入CO2反应生成了碳酸钠和氢氧化铝,该反应的化学方程式为:2NaAlO2+CO2+3H2O═Na2CO3+2Al(OH)3↓.
故答案为:(1)增加反应物接触面积,使反应充分进行;
(2)Fe2O3;
(3)过滤;漏斗;
(4)NaOH;
(5)2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑;
(6)2NaAlO2+CO2+3H2O═Na2CO3+2Al(OH)3↓.
点评 本题以流程图来呈现实验过程的探究性考题,是近几年中考探究题命题特点之一.读懂实验流程图,明确实验步骤和原理,是正确解答此类问题的前提.


科目:初中化学 来源: 题型:实验探究题
| 猜想 | 方案 | 证据 | 结论 |
| 氯化钡可能已完全反应 | 取少量滤液,加入稀硫酸溶液,观察现象 | 无白色沉淀生成 | 氯化钡已完全反应 |
| 硫酸钠可能已完全反应 | 取少量滤液,加入氯化钡溶液,观察现象 | 有白色沉淀生成 | 硫酸钠未完全反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| B. | 向氢氧化钠溶液中滴入硫酸铜溶液产生红褐色沉淀 | |
| C. | 木炭在氧气中燃烧产生浓厚的白烟 | |
| D. | 铁在氧气中剧烈燃烧,生成白色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 反应前物质的组成是混合物 | B. | 反应后生成两种物质 | ||
| C. | 该化学反应是化合反应 | D. | 该反应的本质是原子的重新组合 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 下面是一组实验装置图:
下面是一组实验装置图:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KNO3属于复合肥料 | |
| B. | 所需KNO3的质量是14kg | |
| C. | 主要操作步骤是计量、称量、量取 | |
| D. | 所用玻璃仪器是烧杯、玻璃棒、量筒、胶头滴管 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冰水混合物、蒸馏水、水蒸气都是纯净物 | |
| B. | 松香、玻璃、固态酒精都是非晶体 | |
| C. | 氮气、氦气、氖气等稀有气体都是单质 | |
| D. | 陶瓷、天然橡胶、石墨都是导体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com