
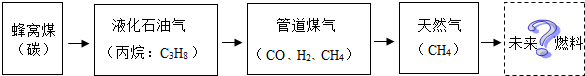
分析 (1)根据燃料燃烧生成二氧化碳解答;由于其制取成本高和贮存困难,作为燃料还不能广泛应用解答;
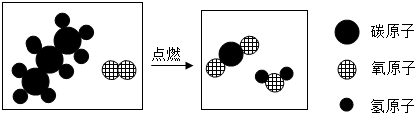
(2)根据化学反应前后原子的种类和数目不变解答;
(3)根据题意,在相同的温度和压强下,相同体积的气体具有相同的分子数,由天然气燃烧的化学方程式、化学方程式的微观意义,列式计算出20L天然气(CH4)充分燃烧消耗O2的体积即可.
解答 解:(1)料燃烧生成二氧化碳,导致温室效应增强;由于其制取成本高和贮存困难,作为燃料还不能广泛应用;
(2)化学反应前后原子的种类和数目不变,该反应前后不变的粒子是C、H、O;丙烷燃烧生成二氧化碳和水,反应的化学方程式为:C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O;
(3)天然气的主要成分是甲烷,燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;微观上可表示点燃条件下,每1个甲烷分子和2个氧气分子反应生成1个二氧化碳分子和2个水分子,即参加反应的甲烷分子和氧分子的个数比为1:2;在相同的温度和压强下,相同体积的气体具有相同的分子数,则20L天然气(CH4)充分燃烧消耗O2的体积可能是40L.
答案:
(1)CO2;制取成本高或储存和运输困难等.
(2)C、H、O
(3)C
点评 化石燃料燃烧能够产生大量污染环境的物质,例如二氧化硫、氮氧化物等,积极开发利用新能源既能够节约化石燃料,又能够防止环境污染.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
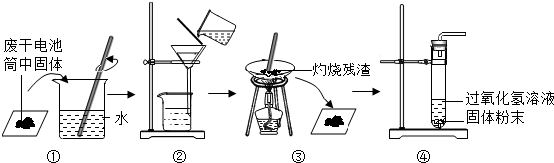
科目:初中化学 来源: 题型:实验探究题
| OH- | Cl- | ${CO}_{3}^{2-}$ | |
| ${NH}_{4}^{+}$ | 溶、挥 | 溶 | 溶 |
| Na+ | 溶 | 溶 | 溶 |
| Zn2+ | 不 | 溶 | 不 |
| Cu2+ | 不 | 溶 | 不 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
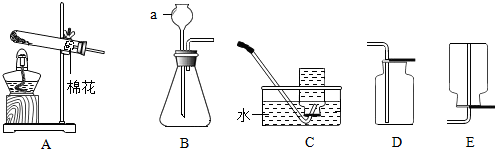
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题



查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
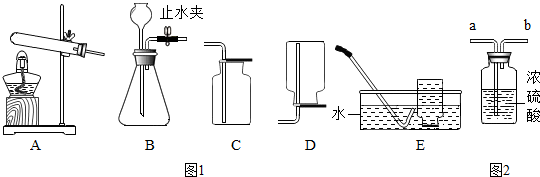
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com