
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/g | 13.9 | 21.2 | 31.6 | 45.3 | 61.3 | 106 | 167 | 203 | 245 |
分析 (1)根据60℃时,硝酸钾的溶解度为106g,进行分析解答.
(2)根据饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}$×100%,进行分析解答.
解答 解:(1)60℃时,硝酸钾的溶解度为106g,其涵义是60℃时,100g水中最多溶解106g硝酸钾,溶液达到饱和状态,则60℃时,在30g水中最多能溶解硝酸钾的质量为106g×$\frac{30g}{100g}$=31.8g.
(2)饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}$×100%,设质量分数为35%的硝酸钾饱和溶液的溶解度为x,则$\frac{x}{x+100g}$×100%=35%,x≈53.8g,由硝酸钾在各个温度下的溶解度如表,60℃时,将质量分数为35%的硝酸钾溶解液逐渐冷却,析出晶体时温度范围应在30~40℃之间.
故答案为:(1)31.8;(2)30~40℃.
点评 本题难度不大,掌握饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}$×100%、溶解度的含义是正确解答本题的关键.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:初中化学 来源: 题型:解答题
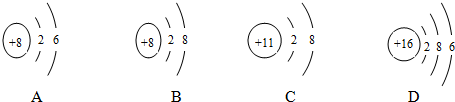
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
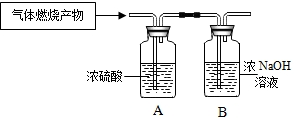 某气体由H2、CO中的一种或两种组成,某化学兴趣小组对该气体的组成进行探究.
某气体由H2、CO中的一种或两种组成,某化学兴趣小组对该气体的组成进行探究.| 现象 | 结论 |
| ①装置A质量增加,装置B质量无变化 | 猜想I成立 |
| ②装置A质量无变化,装置B质量增加 | 猜想Ⅱ成立 |
| ③装置A质量增加,装置B质量增加 | 猜想Ⅲ成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
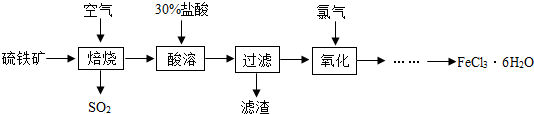
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com