
| 验实号编 | 试 剂 | 前 10min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
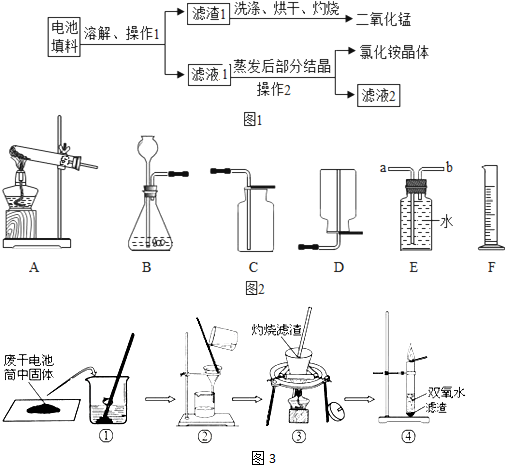
分析 实验1:
过滤可以除去不溶于水的物质;
玻璃棒的用途有搅拌、引流、转移物质等;
加热条件下,炭粉能和空气中的氧气反应生成二氧化碳;
实验2:
根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置;
量筒可以测量液体的体积;
根据实验现象可以判断相关方面的问题;
【实验4探究】
氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气.
解答 解:实验1:
(1)操作1和操作2的名称都是过滤,该操作中玻璃棒的作用是引流.
故填:过滤;引流.
(2)灼烧滤渣l的目的是使炭粉和氧气反应转化成二氧化碳,从而和二氧化锰分离.
故填:使炭粉和氧气反应转化成二氧化碳,从而和二氧化锰分离.
实验2:
(3)①用锌和稀硫酸制取氢气不需要加热,应该用B装置作为发生装置;
氢气密度比空气小,可以用向下排空气法收集,即用D装置收集.
故填:B;D.
②若用排水法收集并测定气体的体积,气体从装置E导管口b进;
选用仪器F测量排出水的体积,仪器F名称是量筒,为了保证测定的准确,出水导管应放在仪器F的上端.
故填:b;量筒;上端.
(4)①比较实验a和实验b,可以得到的结论是锌越纯,与稀硫酸反应的速率越慢.
故填:锌越纯,与稀硫酸反应的速率越慢.
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和c.
故填:a;c.
③控制其他条件相同,需控制的条件是锌的纯度、稀硫酸的浓度、体积等.
故填:锌的纯度.
【数据分析】
①该实验说明:二氧化锰在氯酸钾分解反应前后,质量不变.
故填:质量.
②完全反应后制得氧气的质量是:24.5g+5.5g-20.4g=9.6g,
故填:9.6.
【实验反思】
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较反应速率的大小即可.
故填:反应速率.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3. |

| 实验操作 | 实验现象 | 实验结论 |
| ①取滤渣B于试管中,加入适量稀盐酸 ②将生成的气体通入澄清石灰水 | ①固体减少,有气泡冒出,溶液变为黄色. ②澄清石灰水变浑浊 | 固体中一定含有CaCO3 和Fe2O3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子是化学变化中不能再分的微粒 | B. | 原子在不断地运动着 | ||
| C. | 原子一定是一种比分子更小的微粒 | D. | 有些原子可以直接构成物质. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | 物质的性质与用途 | C | 安全常识 |
| N2性质稳定-填充食品袋防腐 O2支持燃烧-可作发射火箭燃料 | 进入深洞-用手电筒做灯火试验 天然气泄漏-关闭阀门,开窗通风 | ||
| B | 日常生活经验 | D | 构成物质的基本微粒 |
| 生活中硬水软化-煮沸 电视机着火-用水扑灭 | 原子-由原子核和核外电子构成 阳离子-质子数>电子数 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com