
| ���� | 1 | 2 | 3 | 4 |
| ����ϡ���������/g | 70 | 70 | 70 | 70 |
| ʣ����������/g | 18.2 | 16.4 | x | 13.2 |
���� ���ݽ��������ʽ��з������þ����ϡ���ᷴӦ��ͭ����ϡ���ᷴӦ��ʣ��Ĺ����Dz���Ӧ��ͭ����Ϸ�Ӧ�Ļ�ѧ����ʽ���з�����ɣ�
��� �⣺��1�����ݱ����ṩ�����ݿ��Կ���������70g�������ĵĽ���þ�������ǣ�20g-18.2g=1.8g�������μ���70gϡ����ʣ��Ĺ��������Ϊ��16.4g-1.8g=14.6g�����14.6��
��2�����Ĵμ���70gϡ�������ĵ�þ������Ϊ��14.6g-13.2g=1.4g����ʣ���13.2gȫ����ͭ����ͭ��þ��������Ϊ��13.2g����20g-13.2g��=13.2g��6.8g=33��17�����33��17��
��3�����������������Ϊx
Mg+H2SO4�TMgSO4+H2��
24 98
1.8g 70g��x
$\frac{24}{98}=\frac{1.8g}{70g��x}$ x=10.5%
���10.5%��
���� ���⿼����Ǹ��ݻ�ѧ����ʽ�ļ��㣬��ɴ��⣬�������ݱ����ṩ�����ݽ�Ϸ�Ӧ�Ļ�ѧ����ʽ���У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
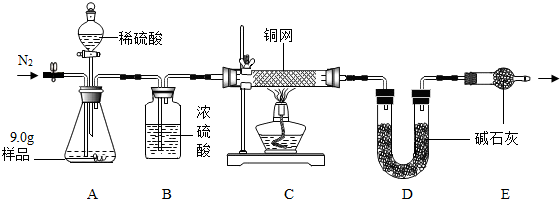
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ȼ�� | B�� | ѹ����������̥���� | ||
| C�� | ��ʯī��Ǧ��о | D�� | ���ʯ����ͷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ܹ������ʣ�ԭ��Ҳ�ܹ������� | |
| B�� | �����ڻ�ѧ�仯��Ҫ�ֽ��ԭ�ӣ������ڻ�ѧ�仯��һ�����ɷ� | |
| C�� | ����������Һ�к������ӡ����������Ӻ�ˮ���ӵ������� | |
| D�� | ���Ӻ����Ӷ�����ԭ���γ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2--2����ԭ�� | |
| B�� | 2H--2����ԭ�� | |
| C�� | Mg2+--þԪ�صĻ��ϼ�Ϊ+2�� | |
| D�� | $\stackrel{+2}{Ca}$--1�������Ӵ�2����λ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 2013��3�£��㽭��ѧʵ���ҵ�����������������IJ���--̼���࣮̼����߱��ߵ��Ժ����ɶ�Ľṹ����Ҫ�ɷ���ʯīϩ�����ܣ����߶��ǵ��ʣ����������ʾ̼������г�ǿ�������������л��ܼ����г��죬���ߵ������������ѱ�������������ߵò��ϣ����ܴﵽ��С�ܶ�0.16���ˡ��������ף�����˵������ȷ���ǣ�������
2013��3�£��㽭��ѧʵ���ҵ�����������������IJ���--̼���࣮̼����߱��ߵ��Ժ����ɶ�Ľṹ����Ҫ�ɷ���ʯīϩ�����ܣ����߶��ǵ��ʣ����������ʾ̼������г�ǿ�������������л��ܼ����г��죬���ߵ������������ѱ�������������ߵò��ϣ����ܴﵽ��С�ܶ�0.16���ˡ��������ף�����˵������ȷ���ǣ�������| A�� | �����ֻ���ش���ʱ���ܳ���������ǵ����� | |
| B�� | �����Ϸ���©���¼�������̼�������ں�����Ѹ������ | |
| C�� | ̼������һ�������¿��Ի�ԭ���������� | |
| D�� | ��ͬ���̼��������С���ܶ�Ϊ0.09ǧ��/���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com