
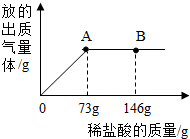
 在烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,向其中逐渐滴加质量分数为10%的稀HCl,放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答:
在烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,向其中逐渐滴加质量分数为10%的稀HCl,放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答:分析 (1)Na2CO3和NaCl组成的固体混合物,只有碳酸钠与稀HCl反应生成氯化钠和水和二氧化碳;
(2)欲知当滴加了73g稀盐酸时,放出气体的总质量,须知此时是否完全反应,然后可根据化学方程式得出得出比例式,即可求出放出气体的总质量;
(3)欲知烧杯中溶液里的溶质,须知此时是否完全反应,反应物是否剩余,再判断溶液中的溶质有哪些物质;
(4)当滴加稀盐酸至图中A点时,烧杯中溶液里溶质的变化是Na2CO3的质量减少至消失、NaCl的质量增加;
(5)根据化学方程式,得到各物质之间的比例式,求出各物质的量,再根据质量守恒定进行计算出溶液质量结合稀释时溶质质量不变来分析.
解答 解:(1)碳酸钠与稀HCl反应生成氯化钠和水和二氧化碳;
73g10%的稀盐酸中含HCl的质量是:73g×10%=7.3g
设放出气体的总质量为x,参加反应的碳酸钠的质量为y.反应生成的氯化钠的质量为z.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 73 117 44
y 7.3g z x
$\frac{73}{7.3g}=\frac{44}{x}$;
解之得x=4.4g;
$\frac{106}{y}=\frac{73}{7.3g}=\frac{117}{z}$
解之得y=10.6g
解之得z=11.7g
(2)由图象可知,生成气体质量(x)的比例式$\frac{73}{7.3g}=\frac{44}{x}$;
(3)因到A点时已完全反应,故到B 点时盐酸有剩余,故烧杯中溶液里的溶质有NaCl、HCl;
(4)当滴加稀盐酸至图中A点时,碳酸钠与稀盐酸反应会不断减少生成氯化钠不断增加,故烧杯中溶液里溶质的变化是Na2CO3的质量减少至消失、NaCl的质量增加;
(5)烧杯里溶液中溶质的质量为:11.7g+(22.3g-10.6g)=23.4g
烧杯里溶液质量为:22.3g+73g-4.4g=90.9g
烧杯里不饱和溶液中溶质的质量分数为:$\frac{23.4g}{90.9g}$×100%=25.7%
设要使溶液中溶质的质量分数为10%,需要再向溶液中加入水的质量为m,
23.4g=(90.9g+m)×10%
m=143.1g;
答案:(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)$\frac{73}{7.3g}=\frac{44}{x}$;
(3)HCl、NaCl;
(4)Na2CO3的质量减少至消失、NaCl的质量增加;
(5)143.1g.
点评 本题要求学生熟悉完全反应的特点,能正确理解溶液和溶质的关系,熟练运用溶质的质量分数进行计算,才能正确答题.


科目:初中化学 来源: 题型:解答题
 ”和“
”和“ ”分别表示氮原子和氢原子,如图是氮气与氢气在高温催化剂条件下发生反应的微观模拟图.请根据此图回答下列问题:
”分别表示氮原子和氢原子,如图是氮气与氢气在高温催化剂条件下发生反应的微观模拟图.请根据此图回答下列问题:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
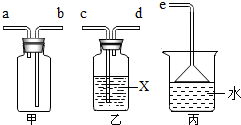 SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.
SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 进入空气不畅通的溶洞,最好用火把进行照明 | |
| B. | 发现厨房煤气泄漏,可立即打开排气扇电源开关 | |
| C. | 用煤炉取暖,可在煤炉上放一壶水以防煤气中毒 | |
| D. | 含糖量较高的粮食,为了防止其霉变可将其放在湿度较大的地方 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用稀盐酸除去铁制品表面的铁锈 | B. | 用一氧化碳冶炼金属 | ||
| C. | 用金属铜制作电路板 | D. | 用熟石灰改良酸性土壤 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 从发生装置中通出的气体往往含有氯化氢气体杂质 | |
| B. | 该实验无明显现象 | |
| C. | 浓盐酸配制稀盐酸时,必须用托盘天平、量筒、烧杯和玻璃棒 | |
| D. | 该反应是复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com