


科目:初中化学 来源: 题型:
| A、不法商贩用过期面粉制作面包 |
| B、在腌渍腌菜时加入亚硝酸钠 |
| C、在酱油中加入铁元素制成“补铁酱油” |
| D、用氢氧化钠治疗胃酸过多 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| X盐 | Y盐 | Z盐 | |
| Ni | 无 | 无 | 有 |
| Zn | 无 | 有 | 有 |
| A、X、Zn、Ni、Y、Z |
| B、X、Y、Ni、Zn、Z |
| C、Z、Zn、Y、Ni、X |
| D、X、Zn、Y、Ni、Z |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 钙 |
| 元素符号 | H | C | O | Cl | Na | Ca |
查看答案和解析>>
科目:初中化学 来源: 题型:
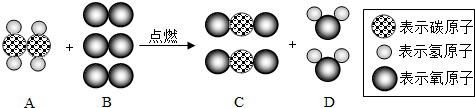
| A、该反应属于氧化反应 |
| B、参加反应的A、B两物质的分子个数比为2:3 |
| C、生成物中C物质与D物质的质量比为22:9 |
| D、反应前后氧元素的化合价发生了改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:
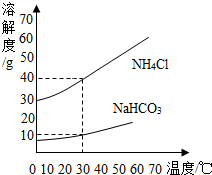 1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | NaOH溶液的质量(g) | 稀盐酸的体积(m L) | 最后所得固体质量(g) |
| 1 | 80.00 | 100.00 | 11.70 |
| 2 | 80.00 | 80.00 | 11.70 |
| 3 | 80.00 | 60.00 | 11.43 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、打开浓盐酸的试剂瓶,看到瓶口冒白烟 |
| B、将打磨光亮的铝丝插入硫酸铜溶液中,看到溶液由蓝色变成浅绿色 |
| C、向硫酸铜溶液中滴入氢氧化钠溶液,有蓝色沉淀生成 |
| D、氯化铵固体和熟石灰混合研磨,生成无色无味的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com