
在“宏观-微观-符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是

A. 硅单质是制造芯片的重要材料,图①是硅原子的结构示意图
B. 图②对应的元素属于金属元素
C. 图②④对应元素组成的化合物是由分子构成的
D. 若图③中x的值为8,则其粒子符号为O2-
C 【解析】A、硅单质是制造芯片的重要材料,硅元素是第14号元素,硅原子中含有14个质子,14个电子,图①是硅原子的结构示意图,正确;B、由粒子结构图可知,该元素是第11号元素钠元素,属于金属元素,正确;C、图②对应元素是钠元素,图④对应元素是氯元素,它们组成的化合物是氯化钠,是由离子构成的,错误;D、图③是第8号元素,氧元素,若x的值为8,则其粒子符号为O2-,正确。故选C。科目:初中化学 来源:广东省深圳市2018届九年级模拟化学试卷 题型:单选题
化学在生产、生活中应用广泛。下列说法错误的是()
A、安全常识 室内煤气泄漏﹣﹣立即打开排风扇 浓硫酸沾到到皮肤上﹣﹣立即用水清洗 | B、元素与人体健康 人体缺铁﹣﹣易引起贫血 人体缺氟﹣﹣易产生龋齿 |
C、生活常识 洗涤剂洗去油污﹣﹣乳化作用 煤炉取暖防中毒﹣﹣开窗通风 | D、环保与物质的利用 减少白色污染﹣﹣使用可降解塑料 减少汽车尾气污染﹣﹣使用乙醇汽油 |
A. A B. B C. C D. D
A 【解析】试题A.室内煤气泄漏时,不能立即打开排风扇,以防点燃煤气而发生事故。浓硫酸沾到到皮肤上应先用布擦去,立即用水清洗。此项不正确。B.人体缺铁易引起缺铁性贫血;人体缺氟质易产生龋齿。此项正确。C.洗涤剂含表面活性分子,有乳化作用,可用于洗去油污;煤炉取暖防易产生无色无味的一氧化碳气体,容易导致中毒;预防时应适当开窗通风。此项正确。D.普通塑料不易降解,可形成白色污染;乙醇燃烧时生成二...查看答案和解析>>
科目:初中化学 来源:山东省滨州市2018年中考化学试卷 题型:填空题
生活处处有化学,请联系学过的化学知识。回答下列问题:
(1)包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等。其中富含糖类的是_________。
(2)人体缺____元素能导致儿童发育不良或佝偻病,老年人会导致骨质疏松。
(3)加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的__________作用。
(4)铁锅容易生锈的主要原因是铁与空气中的________、水蒸气发生了化学反应。
(5)玻璃杯、塑料盆、不锈钢餐具等是生活中常见的日用品,其中属于有机合成材料制成的是____________.
面粉 钙 乳化 氧气 塑料 【解析】(1)包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等。其中富含糖类的是面粉,韭菜主要提供维生素;瘦肉主要提供蛋白质,植物油主要提供油脂,食盐主要提供了无机盐;(2)人体缺钙元素能导致儿童发育不良或佝偻病,老年人会导致骨质疏松;(3)加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的乳化作用;(4)铁锅容易生锈的主要原因是铁与空气中的氧气、水蒸气发生了化学反...查看答案和解析>>
科目:初中化学 来源:山东省滨州市2018年中考化学试卷 题型:单选题
化学使世界变得绚丽多彩。生活中的下列变化没有化学变化发生的是
A. 节日燃放焰火 B. 木炭烤熟食物 C. 西瓜榨成西瓜汁 D. 檀树皮制成宣
C 【解析】物理变化和化学变化的根本区别在于是否有新物质生成,如果有新物质生成,则属于化学变化; 反之,则是物理变化。A. 节日燃放焰火,有新的物质生成,是化学变化; B. 木炭烤熟食物,有新的物质生成,是化学变化; C. 西瓜榨成西瓜汁,没有新的物质生成,是物理变化; D. 檀树皮制成宣,有新的物质生成,是化学变化。故选C。查看答案和解析>>
科目:初中化学 来源:陕西省2018年中考化学试卷 题型:简答题
合理使用化肥可提高农作物产量。下图是生产尿素的微观示意图。回答问题。
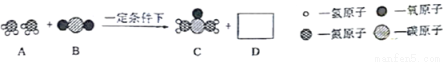
(1)A物质中氮元素的化合价是_____。D物质的化学式是_____。
(2)下列与尿素不属于同类肥料的是_____。
A.NH4HCO3 B.NH4Cl C.K2SO4
-3; H2O; C 【解析】(1)根据化合物各元素正负化合价代数和为0解答;根据质量守恒定律分析解答;(2)根据尿素中含有氮元素解答。(1)由示意图可知,A物质是氨气(化学式为NH3),氨气中氢元素显+1价,故氮元素的化合价为[0-(+1×3)]=-3;反应前后C、H、O、N的原子个数分别为1、6、2、2,1、4、1、2,反应前后相差2个氢原子,1个氧原子,故D物质的化学式为H2O;(2)...查看答案和解析>>
科目:初中化学 来源:福建省泉州市五校2018届九年级联考模拟化学试卷 题型:综合题
某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物。
(一)K2SO4的制备

(1)将CaCO3研成粉末的目的是___________________________________。
(2)M物质的化学式为__________。
(3)反应Ⅲ中相关物质的溶解度如下表。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
反应Ⅲ在常温下能实现的原因是_______________________________________。
(4)上述流程中可循环使用的物质有CO2和_____________(填写化学式)。
(二)研究CaSO4•2H2O加热分解的产物
(5)分离出的CaSO4•2H2O中常含有CaCO3,可用盐酸除去CaCO3,
该反应的化学方程式_______________________________________________。
(6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验。注:碱石灰的主要成分为NaOH和CaO。

① 实验前首先要________________,再装入样品。装置A的作用是_________________。
② 已知:CaSO4•2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解; CaCO3在900℃时分解完全。
现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将______。(填“偏大”、“偏小”或“无影响”)你认为还可选用上述的________________(选填序号)两个数据组合也可求出x:y的值。
(7)CaSO4•2H2O受热会逐步失去结晶水。取纯净CaSO4•2H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。

则G点固体的化学式是_________________。
加快反应速率(或使反应更充分或提高原料的利用率等合理答案均给分) (NH4)2SO4 常温下K2SO4的溶解度小 CaCO3 CaCO3+2HCl=CaCl2+CO2↑+H2O 检查装置的气密性 除去空气中的CO2和H2O 偏小 b、c CaSO4•H2O 【解析】(一)(1)根据将CaCO3研成粉末,碳酸钙与硫酸接触面积更大,其目的是加快反应速率解答;(2)根据质量守恒定律分析解答;(3)...查看答案和解析>>
科目:初中化学 来源:福建省泉州市五校2018届九年级联考模拟化学试卷 题型:单选题
物质的结构决定性质,下列有关说法错误的是( )
A. 过氧化氢与水化学性质不同的原因是由于分子构成不同
B. 钠元素与铝元素化合价不同的原因是由于其原子最外层电子数不同
C. 氢氧化钠与氢氧化钙化学性质相似的原因是其水溶液中都含有OH—
D. 金刚石与石墨物理性质差异较大的原因是由于碳原子不同
D 【解析】A、过氧化氢与水化学性质不同,是因为它们的分子构成不同,不同种的分子性质不同,正确;B、钠元素与铝元素化合价不同,是因为钠原子最外层电子数为1,铝原子最外层电子数为3,最外层电子数不同,正确;C、氢氧化钠与氢氧化钙化学性质相似的原因是其水溶液中都含有OH—,正确;D、金刚石与石墨物理性质差异较大的原因是由于碳原子排列方式不同,错误。故选D。查看答案和解析>>
科目:初中化学 来源:福建省泉州五校2018届九年级联考模拟卷化学试卷 题型:单选题
下列实验进行中的现象或实验原理正确的是( )

A.白磷始终不燃烧

B.小气球变瘪

C.U型管内液面左高右低

D.验证Fe、Cu、Ag的金属活动性强弱
C 【解析】 试题A、根据燃烧的条件分析; B、根据氢氧化钠与二氧化碳反应使瓶内的压强变小分析; C、根据硝酸铵溶于水吸热,使瓶内的压强减小; D、根据金属与盐反应的条件考虑本题,能反应说明该金属排在盐中金属的前面,不反应说明该金属排在盐中金属的后面. 【解析】 A、热水的温度是80℃已经达到白磷的着火点,又与氧气接触,所以可以燃烧,故A错误; B、氢氧...查看答案和解析>>
科目:初中化学 来源:湖北省孝感市2018年中考理综化学试卷 题型:计算题
某化学兴趣小组同学们与老师一起探究铝的化学性质时发现, 铝还能与氢氧化钠溶液反应,其反应的化学方程式为:2A1+ 2NaOH+ 2H2O=2NaAlO2 +3H2↑。现取某氢氧化钠溶液样品50g例入烧杯中,再向其中放入足量打磨好的铝片,生成气体质量与加入铝片质量的变化关系如图所示。

试回答下列问题:
(1)反应完成后生成氢气的质量为__________g。
(2)求原氢氧化钠溶液中氢氧化纳的质量分数为_______。(请写出计算过程)
0.6 16% 【解析】(1)由图中信息知,反应完成后生成氢气的质量为0.6g。 (2)解∶设原氢氧化钠溶液中氢氧化纳的质量分数为x 2A1+ 2NaOH+ 2H2O=2NaAlO2 +3H2↑ 80 6 50g×x 0.6g = ,x=16%。 答∶(1)反应完成后生成氢气的质量为0.6g。(2)原氢氧化钠溶液中氢氧化钠的质量分数为16%。 点睛∶...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com