
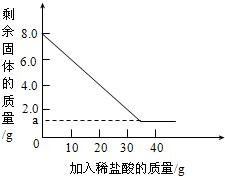
 某化学兴趣小组为了测定当地石灰石的纯度(查资料已知,石灰石中含有二氧化硅,二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).现取用8g该石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸40g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象见下图.
某化学兴趣小组为了测定当地石灰石的纯度(查资料已知,石灰石中含有二氧化硅,二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).现取用8g该石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸40g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象见下图.| 稀盐酸用量 | 剩余固体质量 |
| 第1次加入10g | 6g |
| 第2次加入10g | 4g |
| 第3次加入10g | 2g |
| 第4次加入10g | 1g |
| 7g |
| 8g |
| 100 |
| 73 |
| 2g |
| x |
| 1.46g |
| 10g |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 200 | 200 | 200 | 200 |
| 剩余固体质量(g) | 37.6 | 15.2 | 4 | 4 |

查看答案和解析>>
科目:初中化学 来源: 题型:
| 反应时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
| 烧杯及所盛物质质量/克 | 80.0 | 79.0 | 78.3 | 77.9 | 77.8 | 77.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验.实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止.测得反应前后的有关质量如表:
某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验.实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止.测得反应前后的有关质量如表:| 反应前:整套装置+石灰石样品质量/g | 共加入:稀盐酸质量/g | 反应后:整套装置+锥形瓶中剩余物的质量/g |
| 104.60 | 20.00 | 123.72 |
查看答案和解析>>
科目:初中化学 来源:2013-2014学年江苏省苏州高新区九年级上学期期末考试化学试卷(解析版) 题型:计算题
某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。
实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表:


(1)计算石灰石样品中CaCO3的质量分数。
(2)若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能??? (填“偏大”、“偏小”或“准确”),原因是??? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com