
【题目】阅读下面材料,回答问题。
人类赖以生存的环境由自然环境和社会环境组成。自然环境由生物圈、岩石圈、大气圈、水圈组成(如图所示),四个圈层经过漫长演化,既相对稳定、动态平衡,又相互作用、不断变化,各圈层之间的物质和能量不停循环,这些循环既跟物质的组成、结构和性质有关,也受人类活动的影响,并通过复杂的物理变化和化学变化实现。

(一)内涵决定身份﹣﹣物质的组成与分类
(l)用化学符号填空:
岩石圈中含量最高的金属元素是_____。大气圈中含量最高的物质是_____。水圈中含量最高的元素是_____。土壤中能促进农作物根系发达的元素是_____。
(2)按要求填表:
物质所属圈层 | 物质名称 | 物质的化学式 | 用符号表示构成物质的微粒 | 物质类别 |
生物圈 | 蔗糖 | _______ | _______ | _______ |
大气圈 | 氩气 | _______ | _______ | _______ |
水圈 | 氢氧化钙 | _______ | _______ | _______ |
岩石圈 | _______ | _______ | Na+、SiO32﹣ | _______ |
(二)甲烷﹣﹣小分子,大作为
在如图的四大圈层中,有下列6种物质:①甲烷;②水;③二氯化碳;④一氧化碳;⑤氢气;⑥氧气。构成这些物质的分子虽然简单,但这些物质有的是人类赖以生存的基本物质,有的是物质循环关键物质,有的是人类社会生产活动必需的物质。请回答:
(1)在这6种物质中,元素种类共有_____种,人类的生命活动不可缺少的物质有_____(填化学式,下同),植物生长必需的物质有_____,元素种类完全相同的物质是_____。
(2)甲烷是最重要的基础有机物之一,不仅可做燃料,还能发生如下反应:
①在隔绝空气和1000℃条件下,甲烷分解产生炭黑和氢气;
②在隔绝空气和1500℃条件下,甲烷分解产生乙炔和氢气;
③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳;
④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②~④三个反应的化学方程式:
②_____;
③_____;
④_____;
(3)在反应①~④中,属于置换反应的有_____。
在反应①和②中,反应物相同,而生成物不同,从微观的角度看,是因为反应条件不同导致_____。
③和④两个反应的反应物不同,但生成物相同,从物质组成的角度看,其原因是_____。
在实际生产中,反应③需要按比例控制氧气不能超量,从物质性质的角度看,原因是_____。
(三)柔之力﹣﹣神奇的水溶液
水在生活、生产和科学实验中应用广泛。岩石圈约有四分之三被水覆盖,其中的某些物质被水溶解,其随水的天然循环在水圈中富集,富集后的物质可能再次沉积到岩石圈。
如图是氯化钠和碳酸钠的溶解度曲线。据图回答下列问题:
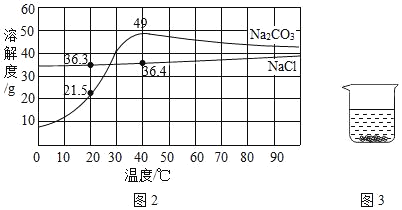
(1)青海湖区的人们有一种经验,冬天捞“碱”、夏天晒盐,这里的“碱”指纯碱,盐指氯化钠,他们所依据的原理是____。
(2)纯碱是一种重要的化工原料,但仅用物理方法从盐湖中“捞碱”远远不能满足需求,工业上主要利用从水圈中获得的食盐来制备纯碱,其反应的化学方程式是_____、_____。
(3)为确定某白色固体是碳酸钠还是氯化钠,在20℃时,取2.5g样品加入盛有10g水的烧杯中,充分搅拌后现象如图所示,则固体粉末是_____。若将该溶液升温到40℃时,则所得溶液溶质质量分数为_____。
(四)金属﹣﹣工业的脊梁
金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制'备金属镁,流程如图所示:
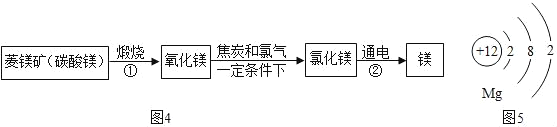
请回答下列问题:
(l)已知①和②属于分解反应,化学方程式分别为_____和_____。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明(用化学方程式表示其制备原理)_____。
(3)如图是镁原子结构示意图,镁化学性质活泼,原因是_____。四大圈层中含有下列物质:①硫酸锌;②氯化钠;③硫酸;④氢氧化钙;⑤氧气。其中能和铁反应的物质有(填序号)_____。
(4)小梅同学将点燃的镁条伸入盛二氧化碳的集气瓶中,看到镁条剧烈燃烧,发出耀眼白光,瓶壁上有黑色物质生成,她认为这种黑色物质是碳单质。在上述过程中,小梅运用的科学方法有_____。
【答案】Al N2 O P C12H22O11 C12H22O11 有机物 Ar Ar 单质 Ca(OH)2 Ca2+、OH﹣ 碱 硅酸钠 Na2SiO3 盐 3 H2O、O2 CO2、H2O、O2 CO、CO2 2CH4 ![]() C2H2+3H2 2CH4+O2
C2H2+3H2 2CH4+O2![]() 4H2+2CO CH4+CO2
4H2+2CO CH4+CO2![]() 2H2+2CO ③ 反应条件不同,原子的结合方式不同,导致分子构成不同;反应物的组成元素相同,反应前后元素的种类不变 超过1400℃,氢气、一氧化碳会与氧气反应 氯化钠溶解度受温度影响较小,夏天温度高,加快水分蒸发,氯化钠容易结晶析出。碳酸钠溶解度受温度影响较大,冬天温度低,易结晶析出 NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl; 2 NaHCO3
2H2+2CO ③ 反应条件不同,原子的结合方式不同,导致分子构成不同;反应物的组成元素相同,反应前后元素的种类不变 超过1400℃,氢气、一氧化碳会与氧气反应 氯化钠溶解度受温度影响较小,夏天温度高,加快水分蒸发,氯化钠容易结晶析出。碳酸钠溶解度受温度影响较大,冬天温度低,易结晶析出 NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl; 2 NaHCO3![]() Na2CO3+CO2↑+H2O Na2CO3 20% MgCO3
Na2CO3+CO2↑+H2O Na2CO3 20% MgCO3![]() MgO+CO2↑ MgC12
MgO+CO2↑ MgC12![]() Mg+C12↑ 3CO+Fe2O3
Mg+C12↑ 3CO+Fe2O3![]() 2Fe+3CO2。 镁原子最外层电子数为2.在化学反应中易失电子 ③⑤ 实验、观察、推理
2Fe+3CO2。 镁原子最外层电子数为2.在化学反应中易失电子 ③⑤ 实验、观察、推理
【解析】
(一)(1)岩石圈中含量最高的金属元素是铝元素,大气圈中含量最高的物质是氮气,水圈中含量最高的元素是氧元素,土壤中能促进农作物根系发达的元素是磷元素,对应的化学符号是Al;N2;O;P;
(2)蔗糖的化学式为C12H22O11;是由蔗糖分子构成的,属于有机物;氩气的化学式为Ar,是由氩原子构成的,属于单质;氢氧化钙的化学式为Ca(OH)2,是由钙离子和氢氧根离子构成的,属于碱类物质;由钠离子和硅酸根离子构成的物质是硅酸钠,其化学式为Na2SiO3,属于盐类物质。
(二)(1)①甲烷中含有碳元素、氢元素;②水中含有氢元素和氧元素;③二氯化碳中含有碳元素和氧元素;④一氧化碳中含有碳元素和氧元素;⑤氢气中含有氢元素;⑥氧气中含有氧元素,所以由三种元素组成;人类的生命活动不可缺少的物质有H2O、O2;植物生长必需的物质有CO2、H2O、O2;元素种类完全相同的物质是一氧化碳和二氧化碳,即:CO、CO2;
(2)②在隔绝空气和1500℃条件下,甲烷分解产生乙炔和氢气,化学方程式为:2CH4![]() C2H2+3H2;③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳,化学方程式为:2CH4+O2
C2H2+3H2;③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳,化学方程式为:2CH4+O2![]() 4H2+2CO;④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳,化学方程式为:CH4+CO2
4H2+2CO;④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳,化学方程式为:CH4+CO2![]() 2H2+2CO。
2H2+2CO。
(3)置换反应是指一种单质和一种化合物反应生成另一种单质和另一种化合物,只有③属于置换反应;反应条件不同,原子的结合方式不同,导致分子构成不同;反应物的组成元素相同,根据质量守恒定律,反应前后元素的种类不变,所以生成物相同;超过1400℃,氢气、一氧化碳会与氧气反应;
(三)(1)溶解度受温度影响较大的物质析出晶体的方法是:降温结晶;溶解度受温度影响较小的物质析出晶体的方法是:蒸发结晶,氯化钠溶解度受温度影响较小,夏天温度高,加快水分蒸发,氯化钠容易结晶析出;碳酸钠溶解度受温度影响较大,冬天温度低,易结晶析出。
(2)氯化钠、水、二氧化碳、氨气反应生成氯化铵和碳酸氢钠,方程式是: NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;碳酸氢钠加热生成碳酸钠、水和二氧化碳,所方程式是:2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
(3)20℃,碳酸钠的溶解度小于25g,氯化钠的溶解度为36g,所以在20℃时,取2.5g样品加入盛有10g水的烧杯中,不能全部溶解的是碳酸钠;将该溶液升温到40℃时,2.5g溶质全部溶解,溶质质量分数为:![]() ×100%=20%;
×100%=20%;
(四)(1)碳酸镁煅烧生成氧化镁和二氧化碳,化学方程式为:MgCO3![]() MgO+CO2↑;氯化镁电解生成镁和氯气,化学方程式为:MgC12
MgO+CO2↑;氯化镁电解生成镁和氯气,化学方程式为:MgC12![]() Mg+C12↑(2)一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式:3CO+Fe2O3
Mg+C12↑(2)一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式:3CO+Fe2O3![]() 2Fe+3CO2,(3)镁原子最外层电子数为2,在化学反应中易失电子;铁可以和氧气反应,铁可以和酸反应,铁可以和盐反应,但铁排在锌后面,与硫酸锌不反应,所以选③⑤;
2Fe+3CO2,(3)镁原子最外层电子数为2,在化学反应中易失电子;铁可以和氧气反应,铁可以和酸反应,铁可以和盐反应,但铁排在锌后面,与硫酸锌不反应,所以选③⑤;
(4)将点燃的镁条伸入盛二氧化碳的集气瓶中,看到镁条剧烈燃烧,发出耀眼白光,瓶壁上有黑色物质生成,这是实验和观察,她认为这种黑色物质是碳单质,这是推理。


科目:初中化学 来源: 题型:
【题目】A、B、C、D、E均为初中化学常见的物质,它们的转化关系如图所示,部分生成物及反应条件已略去.

(1)如果A、B均为黑色固体,C是造成温室效应的主要气体,则E的化学式是 ,A与B反应的化学方程式可能是 .
(2)如果C是一种浅绿色溶液,D是红色固体单质,则E的化学式是 ,A与B反应的化学方程式可能是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c 三种物质的溶解度曲线如下图所示。取等质量![]() ℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至
℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至![]() ℃。下列说法不正确的是
℃。下列说法不正确的是
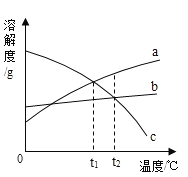
A. 原饱和溶液中,溶质的质量分数 a>b="c"
B. 恢复至 t2℃时,析出溶质的质量 a>b=c
C. 恢复至t2℃时,三种溶液一定都是饱和溶液
D. 若继续降温至 t1℃,三种溶液一定都是饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学做“证明鸡蛋壳的主要成分是碳酸盐,并收集纯净的气体”的实验。设计了如下方案进行实验:
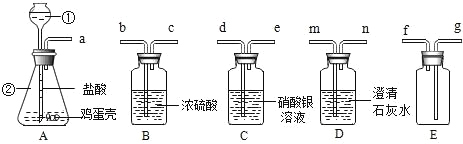
(1)写出所标仪器的名称:①_____、②_____。
(2)根据我们所学的知识,你认为A装置和_____装置相连进行实验,就可以检验鸡蛋壳的主要成分是碳酸盐。写出D装置中发生反应的化学方程式:_____。
(3)写出用A装置还可以制取 的 日 常生活中一种常见气体的化学反应方程式:_____。并说出它的一个重要用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石墨烯是一种革命性材料,具有优异的光学、电学和力学特性。图为金刚石、石墨和石墨烯的结构模型图,图中小球代表碳原子。下列说法正确的是( )
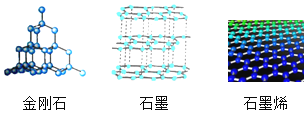
①石墨烯是一种新型化合物
②三种物质分别在足量的氧气中完全燃烧的产物相同
③金刚石和石墨烯是组成相同但结构不同的两种物质
④石墨烯有超强的导电性和导热性,说明石墨烯的化学性质和金属相似
A. ①④ B. ②③ C. ①③ D. ②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学学习小组的同学在学习了《常见的酸》以后,对蚊虫分泌的让人痛痒不止的蚁酸产生了兴趣。他们在老师指导下对蚁酸进行探究。
(查阅资料)蚁酸的主要成分是甲酸,甲酸的化学式为HCOOH;甲酸溶于水,在一定条件下发生分解反应生成两种氧化物。
(提出问题)甲酸溶液是否具有酸性?
(实验与结论)向盛有甲酸溶液的试管中滴加紫色石蕊溶液,观察到溶液颜色变成红色,说明甲酸溶液显____性。
(提出问题)甲酸分解生成的两种氧化物是什么?
(推断与猜想)
⑴小组同学根据甲酸中含有氢元素,推测出生成物中含有水。
⑵他们对另一种氧化物提出两种猜想:猜想①:二氧化碳;猜想②:一氧化碳。
(实验与结论)
为了证明自己的猜想,他们将甲酸分解产生的气体通过如下图所示的装置(铁架台已略去)。
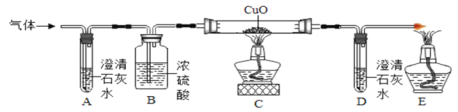
观察到的实验现象如下:
Ⅰ.装置A中澄清石灰水无明显变化。
Ⅱ.装置C中的黑色粉末变红色。
Ⅲ. 装置D中澄清石灰水变浑浊。
(实验结论)甲酸具有酸性,在一定条件下分解生成水和_______。
(拓展延伸)人被蚊虫叮咬后,在其叮咬处涂抹______________可减轻痛痒。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学中常见化合物间的相互关系,且分别是由H、C、O、Cl、Na、Ca中几种元素组成。其中D、E属于氧化物,B、G是同一类别物质,胃液中含有少量的A,可帮助消化,F是常用的补钙剂的主要成份。图中“﹣”表示两端的物质能发生化学反应,“”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去。
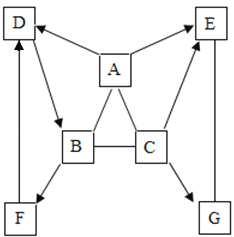
(1)写出物质F的化学式_____。
(2)A和B之间反应的化学方程式_____。
(3)C→G反应的化学方程式_____。
(4)从微观角度分析C→E反应的本质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】吸烟有害健康。香烟的烟气中含有毒的尼古丁,其结构式如图,下列关于尼古丁的叙述正确的是![]()
![]()

A. 尼古丁分子中质子数与电子数相等
B. 尼古丁分子中氮、氢两种元素质量比为1:1
C. 尼古丁是由碳、氢、氮三种原子构成的
D. 尼古丁属于有机高分子化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映其对应关系的是

A. ①表示向一定量的稀硫酸中加入足量的锌粒
B. ②表示向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液
C. ③表示向一定量的氢氧化钠溶液中滴加稀硫酸
D. ④表示将等质量的大理石分别与足量的等体积等溶质质量分数的稀盐酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com