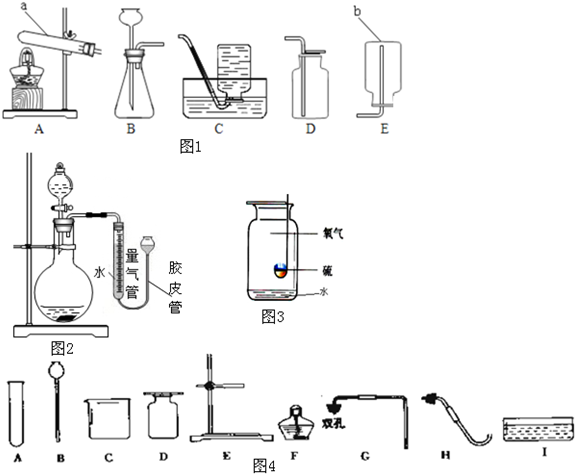
工业上常用分离液态空气法制取氧气,实验室常用物质分解的方法制氧气(图1).
(1)工业制氧气是
物理
物理
(填“物理”或“化学”)变化.
(2)写出仪器名称:a
试管
试管
,b
集气瓶
集气瓶
.
(3)用过氧化氢溶液和二氧化锰制取氧气时,所选用的发生装置是
B
B
(填序号),
其反应的符号表达式是
,
其收集装置不能选
E
E
(填序号).
某同学想用D装置收集氧气一瓶,实验中用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃.其原因可能是
装置漏气或收集时间不够长或H2O2变质或H2O2浓度低等
装置漏气或收集时间不够长或H2O2变质或H2O2浓度低等
.
(4)写出用A装置制取氧气的符号表达式
.
(5)若采用如图2所示装置制取氧气并测定其体积,
实验前应检查装置的气密性.为了准确测定氧气的体积,有人提出读数时应该注意以下事项:
①容器中气体必须冷却至室温;
②长颈漏斗不能倾斜;
③必须使量气管和长颈漏斗两边液面相平;
④视线应与液体凹液面最低处保持水平.
你认为必须要做到的是
①③④
①③④
(填序号).
(6)①若用装置B制氧气,反应通常很剧烈,据此提出实验安全注意事项是
A D
A D
(填序号)
A.更换部分仪器,控制液体的加入速度 B.用体积小的广口瓶
C.加热反应物 D.减小过氧化氢浓度
②用此法代替高锰酸钾加热制氧气,优点是
A B
A B
(填序号)
A.操作简单 B.不需加热 C.需加热 D.生成物中只有氧气
(7)收集好氧气后,小雨同学接着做了“硫在氧气中燃烧”实验.(如图3)
①小雨把观察到现象作了如下记录,其中正确是
AC
AC
(填字母序号).
A.点燃硫的时候,可观察到硫先融化为液态然后开始燃烧
B.硫在空气中点燃后产生淡蓝色火焰,生成二氧化硫
C.硫在氧气中燃烧比在空气中剧烈,产生蓝紫色火焰,放出有刺激性气味气体.
②请写出硫燃烧的符号表达式:
;
该反应的反应类型是:
化合反应
化合反应
.
③在实验前,集气瓶内会提前预留少量的水,其目的是:
吸收二氧化硫,防止污染
吸收二氧化硫,防止污染
.
④该实验能否直接用于“测定空气中氧气含量”的实验?
不能
不能
;
你的理由是:
生成气体,压强变化不大
生成气体,压强变化不大
.
(8)通过以上知识的巩固,老师出了一道检测题,请分析.
选用了图4中仪器A、D、E、F、I设计一套制取氧气的装置,他还需选用的仪器是
H
H
.

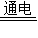 Mg+Cl2↑,该反应属于( )
Mg+Cl2↑,该反应属于( ) Mg+Cl2↑是由一种物质生成两种或两种以上的其它物质的化学反应,应是分解反应.
Mg+Cl2↑是由一种物质生成两种或两种以上的其它物质的化学反应,应是分解反应.

 试回答:
试回答: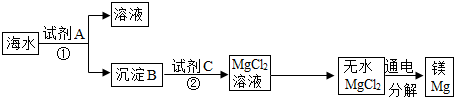

 (2013?丰台区二模)金属材料在生产、生活中有着广泛的应用.
(2013?丰台区二模)金属材料在生产、生活中有着广泛的应用.