
(5分)元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究:

⑴第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
⑴ 非金属 ;得 ;⑵ 最外层电子 ;⑶ 电子层数递增或最外层电子数相等或从上到下核电荷数增大等(只要合理均可)⑷ 逐渐减小
【解析】
试题分析:(1)根据原子最外层电子数的特点分析,非金属元素的原子最外层电子的数目一般多于4个,在化学反应中容易得到电子达到稳定结构;金属元素的原子最外层电子的数目一般少于4个,在化学反应中容易失去电子达到稳定结构,第16号元素的原子最外层电子数为6,故属于非金属元素,在化学反应中容易得到2个电子。
(2)原子核外最外层电子数少于4个,一般容易失去电子形成阳离子;原子核外最外层电子数多于4个的,一般容易得到电子形成阴离子;原子核外最外层电子数为8个(只有一层的有2个电子)的,化学性质一般比较稳定,不容易发生化学变化,故元素的化学性质与原子核外的最外层电子数有密切关系。
(3)根据元素周期表分析,在同一族中(一竖行),从上到下核电荷数依次增大,各元素的原子的电子层数依次递增,但最外层电子数相等。
(4)根据题意,同一周期中,“核电荷数逐渐增大,核对核外电子的引力逐渐增大,原子半径逐渐减小”,所以从11~17号元素原子半径也是逐渐减小。
考点:元素周期表的特点及其应用,原子的定义与构成,核外电子在化学反应中的作用,原子结构示意图与离子结构示意图
点评:理解和熟练掌握元素周期表的特点及其应用,是解答本题的关键。


科目:初中化学 来源:2013届山东省滨州市滨城区第三中学九年级上学期期末考试化学试卷(带解析) 题型:填空题
(5分)元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究: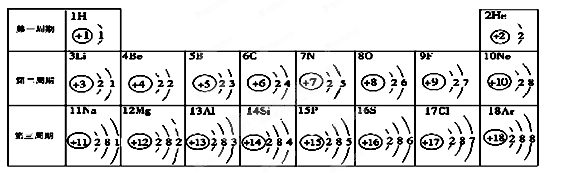
⑴第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
查看答案和解析>>
科目:初中化学 来源:2012-2013学年陕西省西安高新第二学校九年级上学期期中检测化学试卷(解析版) 题型:填空题
(4分)元素周期表是化学学习和研究的重要工具。下图是元素周期表的一部分。
|
1 H 1.008 |
|
2 He 4 .003 |
|||||
|
3 Li 6 .941 |
4 Be 9 .012 |
5 B 10.81 |
6 C 12.01 |
7 N 14. 01 |
8 O 16.00 |
9 F 19.00 |
10 Ne 20.18 |
|
11 Na 22.99 |
12 Mg 24.31 |
13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18 Ar 39.95 |
(1)从表中查出硅(Si)元素的相对原子质量为 ;
(2)6~11号元素中属于金属元素的有 (填元素符号);
(3)表中不同种元素最本质的区别是 (填序号);
A.质子数不同 B.中子数不同 C.相对原子质量不同 D.核外电子数不同
(4)科学家宣布已经人工合成了第116号元素,则此元素的核电荷数是 。
查看答案和解析>>
科目:初中化学 来源:2011-2012学年广东省汕头市潮南区九年级中考模拟考试化学试卷(解析版) 题型:填空题
(4分) 元素周期表是学习和研究化学的重要工具。下表是元素周期表中的一部分,请按表中信息填空:?
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
O |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10Ne 氖 20.18 |
|
3 |
11Na 钠 22.99 |
12Mg ?镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)查找出原子序数为10的元素的相对原子质量 。?
(2)硫元素的原子结构示意图为 ,该元素的原子核外有
个电子层,它属于
元素(填“金属”、“非金属”),其化学性质比较活泼,在化学反应中易 (填“得”、“失”)电子。
,该元素的原子核外有
个电子层,它属于
元素(填“金属”、“非金属”),其化学性质比较活泼,在化学反应中易 (填“得”、“失”)电子。
查看答案和解析>>
科目:初中化学 来源:2010-2011学年广西百色市毕业暨升学考试化学试卷 题型:填空题
(5分)元素周期表和化学用语都是学习化学的重要工具,回答下列问题:
|
3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
|
11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
(1)同一周期(横行)中,相邻两种元素的质子数之差为 ;磷元素原子核外电子数为 ;
(2)12号元素的单质在空气中燃烧时,也发生如下反应:2Mg + CO2 点燃 C +2MgO ,该反应中发生还原反应的物质是 ;9号元素的气体单质(F2)常温下与水发生反应,生成氢氟酸(HF)各另一种无色气体,该反应的化学方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com