
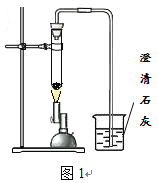
【题目】研究小组进行木炭还原氧化铁的探究活动。将木炭、氧化铁及试管充分烘干,并将木炭和氧化铁混合均匀、研磨。取适量上述混合物于试管中,用图1所示的装置加热(试管竖直向上,可使加热时的热量尽少散失)。
【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】
![]() 铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁。铁的氧化物及其部分性质如下:
铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁。铁的氧化物及其部分性质如下:
![]() 为红色固体;
为红色固体; ![]() 和
和![]() 均为黑色固体。其中,
均为黑色固体。其中,![]() 具有很好的磁性,能被磁铁吸引。三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
具有很好的磁性,能被磁铁吸引。三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl ══ 2FeCl3+3HO
Fe3O4+8HCl ══ 2FeCl3+FeCl2+4H2O
FeO+2HCl ══ FeCl2 + H2O
黄色的![]() 溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验
溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验![]() ;
;![]() 溶液遇单质铁发生反应:2FeCl3 + Fe = 3FeCl2,溶液变为浅绿色。
溶液遇单质铁发生反应:2FeCl3 + Fe = 3FeCl2,溶液变为浅绿色。
【猜想】固体X可能含有:①![]() ②
②![]() ③
③![]() ④ ⑤
④ ⑤![]()
【实施实验】
目的:确定固体X的组成。
步骤 | 操作 | 主要现象 | 结论 |
I | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引。 | 部分固体被吸引到磁铁上 | 可能有 |
II | 取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热。 | 固体剧烈燃烧, b中溶液变浑浊 | 一定有 |
III | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸。 | 无明显现象 | 一定没有 |
IV | 取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸。 | 产生 。 | 一定有 |
V | 在步骤IV所得溶液中逐滴加入 。 | 溶液不变红色 | 一定没有 |
【反思改进】
同学们讨论发现,用上述实验方法不能确定固体X中一定没有![]() ,理由是 。
,理由是 。
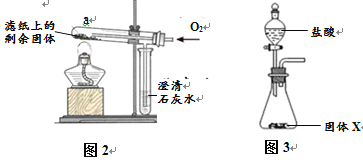
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
步骤 | 操作 | 数据 |
I | 重新取部分冷却至室温的固体X,称量其质量为m1。 | m1 = 17.9 g |
II | 将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量m3。 | m2 = 317.9 g m3 = 317.3.g |
III | 将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4。 | m4 = 1.1 g |
【获得结论】
(1)为确定固体X中是否含![]() ,m1~m4中应该用到的数据有 。
,m1~m4中应该用到的数据有 。
(2)固体X的成分及质量分别是 。
【答案】【猜想】④![]() ;【实施实验】III.
;【实施实验】III. ![]() 和
和![]() ;IV.气泡;V.
;IV.气泡;V.![]() 溶液;【反思改进】固体X中如果含有
溶液;【反思改进】固体X中如果含有![]() ,步骤V中加入盐酸后,由于铁与氯化铁反应生成氯化亚铁,遇硫氰化钾溶液也不变为血红色.【获得结论】(1)m1、m2、m3和m4;(2)
,步骤V中加入盐酸后,由于铁与氯化铁反应生成氯化亚铁,遇硫氰化钾溶液也不变为血红色.【获得结论】(1)m1、m2、m3和m4;(2)![]() :1.1g;
:1.1g;![]() :16.8g
:16.8g
【解析】【猜想】根据质量守恒定律可知剩余固体X中可能还含有![]() ;
;
【实施实验】III. 因为氧化亚铁和稀盐酸反应生成氯化亚铁,使溶液呈浅绿色,氧化铁与稀盐酸反应生成氯化铁,使溶液呈黄色,所以如果取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸,没有明显现象,说明一定没有![]() 和
和![]() ;IV.因为铁与稀盐酸反应生成氢气,所以取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸,如果有气泡产生,则固体中一定含有铁;V. 因为四氧化三铁与稀盐酸反应生成氯化铁和氯化亚铁及水,且黄色的
;IV.因为铁与稀盐酸反应生成氢气,所以取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸,如果有气泡产生,则固体中一定含有铁;V. 因为四氧化三铁与稀盐酸反应生成氯化铁和氯化亚铁及水,且黄色的![]() 溶液中滴入无色的
溶液中滴入无色的![]() 溶液,溶液变为红色,所以在步骤IV所得溶液中逐滴加入
溶液,溶液变为红色,所以在步骤IV所得溶液中逐滴加入![]() 溶液,若固体中不含有四氧化三铁,则溶液不变红色;
溶液,若固体中不含有四氧化三铁,则溶液不变红色;
【反思改进】又因为![]() 溶液遇单质铁发生反应:
溶液遇单质铁发生反应:![]() 可知,如果固体X中含有
可知,如果固体X中含有![]() ,步骤V中加入盐酸后,由于铁与氯化铁反应生成氯化亚铁,遇硫氰化钾溶液也不变为血红色.
,步骤V中加入盐酸后,由于铁与氯化铁反应生成氯化亚铁,遇硫氰化钾溶液也不变为血红色.
【获得结论】(1)要确定固体X中是否含![]() ,由表格中的数据可知m1是固体总质量,m2和m3的质量差为铁与酸反应生成的氢气质量,即:317.9g-317.3g=0.6g;m4是不与酸反应的碳的质量,即17.9g固体中含有1.1g的碳;因此要测定固体X中是否含有四氧化三铁,需要m1、m2、m3和m4四个数据.
,由表格中的数据可知m1是固体总质量,m2和m3的质量差为铁与酸反应生成的氢气质量,即:317.9g-317.3g=0.6g;m4是不与酸反应的碳的质量,即17.9g固体中含有1.1g的碳;因此要测定固体X中是否含有四氧化三铁,需要m1、m2、m3和m4四个数据.
设固体混合物中含有铁的质量为x,
![]()
56 2
x 0.6g
56:x=2:0.6g x=16.8g
所以固体X中含有![]() :1.1g;
:1.1g;![]() :16.8g,不含有四氧化三铁.
:16.8g,不含有四氧化三铁.
试题分析:【猜想】根据质量守恒定律进行猜想;【实施实验】根据氧化亚铁、四氧化三铁、铁与稀盐酸的反应现象,以及氯化铁与氰化钾溶液反应的颜色变化分析;【反思改进】根据铁与氯化铁反应会生成氯化亚铁,氯化亚铁遇氰化钾不变红色分析;【获得结论】根据表格中的数据可知m1是固体总质量,m2和m3的质量差为铁与酸反应生成的氢气质量,即:317.9g-317.3g=0.6g;m4是不与酸反应的碳的质量,即17.9g固体中含有1.1g的碳分析;根据反应中生成氢气的质量可以计算固体中铁的质量,根据铁和碳的质量可以判断固体中是否含有四氧化三铁.


科目:初中化学 来源: 题型:
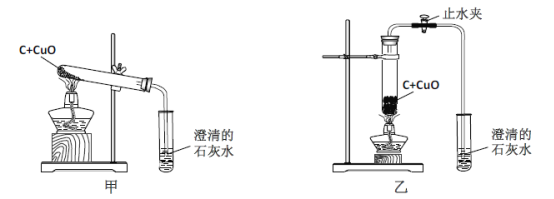
【题目】某化学兴趣小组按照课本实验方法(如下图),做木炭与氧化铜反应的实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。
【提出问题】暗红色的固体是什么?如何选择合适条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有+1 和+2 两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4 或-4。
【猜想与假设】
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为 。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象
更加明显,减少出现暗红色固体的情况。
【分析与交流】
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是 ;反应的化学方程式为 。
(2)小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的好处是 。
【实验与结论】
同学们决定按改进后的方案进行实验,他们在检验了乙 后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时, (填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是 (填“吸”或“放”)热反应。待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
查看答案和解析>>
科目:初中化学 来源: 题型:
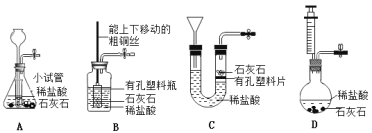
【题目】根据装置图回答。

Ⅰ.写出图中仪器a的名称是 ,仪器b的名称 。
Ⅱ.在图中若用无水醋酸钠和碱石灰两种固体药品加热制取甲烷气体,可选用的发生装置是 ;装置B 和C都可以用过氧化氢溶液和二氧化锰制取氧气,写出该反应的化学方程式 ;装置B和C相比,B装置的优点是 。
Ⅲ.以下收集装置中能用于收集氧气的是 。

Ⅳ.以下具有启普发生器功能的简易气体发生装置是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将铁粉加到一定量的硝酸银、硝酸铜和硝酸锌的混合溶液中,充分反应后过滤,在滤渣中加入稀盐酸,无明显现象。则所得滤液中
A.只含有硝酸锌 B.一定含有硝酸锌和硝酸亚铁
C.一定没有硝酸银 D.一定没有硝酸银和硝酸铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验得出的结论或说法不合理的是( )
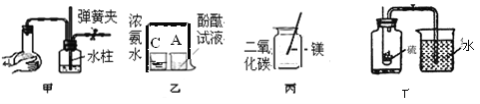
A.甲装置中玻璃导管内水柱上升,说明此装置气密性良好
B.乙实验中A烧杯中酚酞试液变红,可以说明微粒是不停运动的
C.丙实验中镁在二氧化碳中剧烈燃烧,说明助燃物不仅仅是氧气
D.丁实验中可用硫燃烧来测定空气中氧气的体积含量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com