
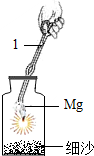
 在集气瓶内放入一装有少量酒精(C2H5OH)的蒸发皿,先点燃蒸发皿内的酒精,再将经打磨过的光量镁条伸入集气瓶内点燃,可看到镁条剧烈燃烧,在瓶底白色固体粉末中夹杂着少量黑色固体,用足量的盐酸处理,结果发现白色物质溶解,黑色物质不溶,由此他猜测:黑色物质是原来镁条中所含的杂质,乙同学没有轻易赞同甲同学的意见,他通过查找资料,知道,镁与空气中的O2、N2、CO2都会发生反应,他推断:这黑色物质是碳,请回答下列问题:
在集气瓶内放入一装有少量酒精(C2H5OH)的蒸发皿,先点燃蒸发皿内的酒精,再将经打磨过的光量镁条伸入集气瓶内点燃,可看到镁条剧烈燃烧,在瓶底白色固体粉末中夹杂着少量黑色固体,用足量的盐酸处理,结果发现白色物质溶解,黑色物质不溶,由此他猜测:黑色物质是原来镁条中所含的杂质,乙同学没有轻易赞同甲同学的意见,他通过查找资料,知道,镁与空气中的O2、N2、CO2都会发生反应,他推断:这黑色物质是碳,请回答下列问题:分析 (1)根据实验室常用仪器的名称,以及先点燃酒精,燃烧放出大量的热并且生成二氧化碳,从而引燃镁条,生成的二氧化碳和镁反应;
(2)根据做铁丝实验时试剂瓶铺有细砂作用一样进行分析;
(3)根据镁条能与盐酸反应,若镁条全反应没有剩余,证明不含杂质进行分析.
解答 解:(1)仪器1的名称是坩埚钳,先点燃酒精,燃烧放出大量的热并且生成二氧化碳.先点燃坩埚内的酒精燃烧产生的热量点燃镁条,酒精燃烧产生的CO2作为后续反应需要的反应物;
(2)在验证氧气与铁反应的实验中也在集气瓶底铺少量的细砂,作用和这里是一样的,防止融熔融物溅落瓶底,使集气瓶炸裂;
(3)镁条中若含有杂质不能和酸反应,将镁条直接与过量(或足量)的盐酸反应,镁条完全溶解,若无黑色物质残留,说明甲同学的猜测不能成立.
故答案为:(1)坩埚钳,酒精燃烧产生的CO2作为后续反应需要的反应物,酒精燃烧产生的热量点燃镁条;
(2)防止融熔物溅落瓶底,使集气瓶炸裂;
(3)取镁条浸入足量的盐酸中,若镁条全部溶解,则甲同学的猜想不正确.
点评 典型的信息给予题,只有熟练掌握物质的性质才能正确快速的得出正确答案.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
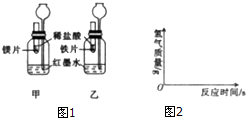 控制变量法是常用的化学学习方法,下面是某小组探究活动的过程:已知试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.在室温条件下进行如图1所示实验.
控制变量法是常用的化学学习方法,下面是某小组探究活动的过程:已知试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.在室温条件下进行如图1所示实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向上排空气法 | B. | 向下排空气法 | ||
| C. | 排水法 | D. | 排水法或向上排空气法 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
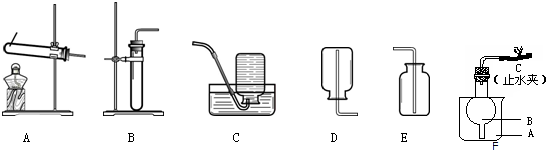
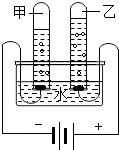 用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )
用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )| A. | ①②③④ | B. | ①② | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
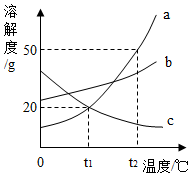 如图是三种固体物质的溶解度曲线.
如图是三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 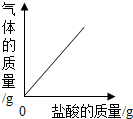 向一定质量的碳酸钙中逐滴滴加稀盐酸 | |
| B. | 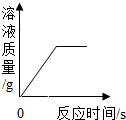 向一定量的稀硫酸中加入锌粉至过量 | |
| C. | 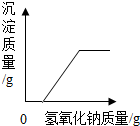 向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液 | |
| D. | 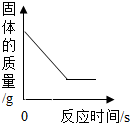 向一定量二氧化锰固体中加入过氧化氢溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com