
| A. | 16g | B. | 8g | C. | 5.6g | D. | 无法计算 |
分析 根据四氧化三铁、氧化铁、碳酸亚铁组成的混合物,通入H2,加热,化学反应前后元素质量守恒,得到5.6g铁粉即为mg混合物中铁元素的质量;混合物与盐酸反应,再加热蒸干并灼烧,最后得到的固体为氧化铁,根据化学反应前后元素质量守恒,最后得到氧化铁中铁元素的质量即为混合物中铁元素的质量,即可解答.
解答 解:根据分析可知,化学反应前后元素质量守恒,
最后得到的氧化铁的质量:5.6g÷$\frac{56×2}{56×2+16×3}$×100%×$\frac{2mg}{mg}$=16g;
答案:A.
点评 考查混合物的计算,难度中等,利用元素守恒判断铁的物质的量是解题关键,注意守恒思想的运用.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
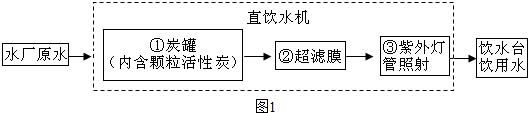
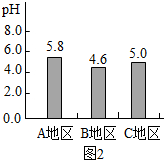
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com