
【题目】某碳酸钠样品中混有一定量的氯化钠固体和不溶于水也不与酸反应的杂质,为测定碳酸钠的纯度,化学兴趣小组做了如下的实验:
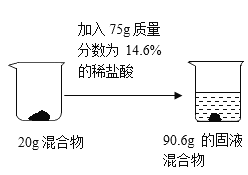

(1)请写出发生反应的化学方程式____________。
(2)根据已知条件,写出求解20g固体中参加反应的物质质量的比例式_____________。
(3)固体混合物中碳酸钠的纯度为________。
(4)若用36.5%的浓盐酸配制实验所需的稀盐酸,则需要水的质量为______________。
(5)若向最终滤液中加入12.15g水,所得不饱和溶液中溶质质量分数为_______________。
【答案】(1)Na2CO3+2HCl=2NaCl+ H2O+ CO2↑
(2)106∶44=x∶4.4g
(3)53%
(4)45g
(5)17.55%
【解析】
(1)根据题意,实验中发生的化学反应是碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式是:Na2CO3+2HCl=2NaCl+ H2O+ CO2↑。
(2)根据已知条件,20g样品中加入75g14.6%的稀盐酸充分反应后,得到90.6g固液混合物,根据质量守恒定律,反应中生成二氧化碳质量为:20g+75g-90.6g=4.4g。
设生成4.4g二氧化碳,消耗碳酸钠的质量为x,同时消耗14.6%的盐酸质量为y,生成氯化钠质量为z。
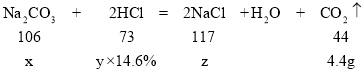
![]() 解得x=10.6g
解得x=10.6g
![]() 解得y=50g
解得y=50g
![]() 解得z=11.7g
解得z=11.7g
根据计算结果,20g固体和75g14.6%的稀盐酸反应后,盐酸有剩余,故20g样品中碳酸钠全部参加反应,20g固体中参加反应的物质质量的比例式是:![]() 。
。
(3)根据上述计算结果,固体混合物中碳酸钠的纯度为:![]() 。
。
(4)根据稀释前后溶质质量不变,设需要36.5%的浓盐酸质量为m。
m×36.5%=75g×14.6%,解得m=30g
则用36.5%的浓盐酸配制实验所需的稀盐酸,则需要水的质量为:75g-30g=45g。
(5)设5.3g碳酸钠和盐酸反应生成的氯化钠质量为a,同时生成二氧化碳质量为b。
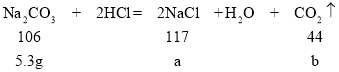
![]()
解得a=5.85g,b=2.2g
则向最终滤液中加入12.15g水,所得不饱和溶液中溶质质量分数为:![]() 。
。


科目:初中化学 来源: 题型:
【题目】复分解反应是我们学过的化学基本反应类型之一。
(1) 写出下列反应的化学方程式。
①氯化钡溶液与硫酸钠溶液混合:_________________________________________;
②碳酸钠溶液与稀盐酸混合:_________________________;
③氢氧化钡溶液与稀硝酸混合:______________________________。
(2)你想过上述复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合。如上述反应①中,实际参加反应的离子Ba2+和SO42-,而Cl-、Na+是“旁观者”,并没有参加反应。请你分析上述反应②中实际参加反应的离子是__________________;上述反应③中实际参加反应的离子是______________________________________________。
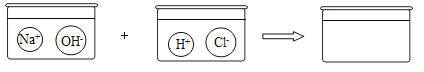
(3)请根据你的想象,在图中右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同。已知C、丙均为黑色粉末,C和E在高温条件下可生成丙和D,其余反应条件、部分反应物和生成物均已略去。试推断:
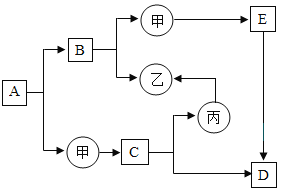
(1)写出有关物质的化学式:甲__________,E___________.
(2)写出下列化学方程式C+E→丙+D____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学,为了比较金属 R 与铁、铜的金属活动性强弱,进行如下探究活动:
(査阅资料)铁的活动性比铜强。
(进行猜想)对三种金属的活动性顺序做出如下猜想: 猜想一:R>Fe>Cu;猜想二:_______________; 猜想三:Fe>Cu>R。
(收集证据)为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究。
主要操作 | 主要现象 | 实验结论 | ||
甲 | 将打磨好的R 丝插入盛有硫酸铜溶液的试管中 | ____________ | 猜想一正确 | |
乙 | 将粗细相同打磨好的 R 丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R 丝表面产生气泡速率比铁丝表面产生气泡速率_____________( 填 “快”或“慢”) | ||
丙 | 将粗细相同打磨好的 R 丝、铁丝,分别在空气中点燃 | R 丝在空气中剧烈燃烧,铁丝在空气中_______________ | ||
写出铁丝在氧气中燃烧的化学方程式:________________。
(交流反思)三位同学交流讨论后认为,比较金属活动性强弱的方法有多种。
(归纳总结)他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与______________是否反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是氮气和氢气发生反应的微观模拟图,请从微观角度回答下列问题:
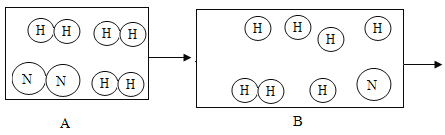
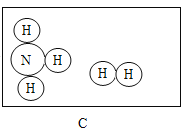
(1)请在图中相应的位置补充相关粒子图形,使其表示正确____________。
(2)该变化前后没有发生改变的粒子__________________。
(3)生成物属__________________(选填“单质”、“化合物”或“混合物”) 。
(4)画出比氮元素多一个周期多一个族的元素的原子结构示意图__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是氢气和氯气发生反应的微观模拟图,“![]() ”代表氢原子,“
”代表氢原子,“![]() ”代表氯原子,请回答下列问题:
”代表氯原子,请回答下列问题:
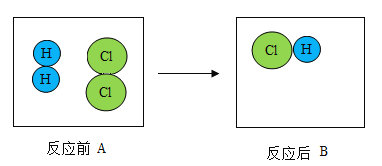
(1)在B图中将相关粒子图形补充完整_____。
(2)A中两种分子的相同点是_____。
(3)某元素的原子比一个B分子少两个质子,画出该原子的离子结构示意图_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文(以下材料来自百度科普材料整理)。
新型冠状病毒肺炎及预防
1965年,分离出第一株人的冠状病毒。由于在电子显微镜下可观察到其外膜上有明显的棒状粒子突起,使其形态看上去像中世纪欧洲帝王的皇冠,因此命名为“冠状病毒”。
2020年2月11日,世界卫生组织总干事谭德塞在瑞士日内瓦宣布,将新型冠状病毒感染的肺炎命名为“COVID-19”。“COVID-19”是一种急性呼吸道传染病。
新冠肺炎一般症状:发热、乏力、干咳、逐渐出现呼吸困难。部分患者起病症状轻微,无发热。少数患者伴有鼻塞、流涕、咽痛和腹泻等症状。严重者死亡。
目前已有确切的证据表明可以人传人。目前所见传染源主要是新冠肺炎患者。无症状感染者也可能成为传染源。新冠肺炎的主要传播途径是经呼吸道飞沫传播,亦可通过接触传播。气溶胶和消化道等传播途径尚待明确。目前新冠肺炎的治疗没有特效药。
在日常生活中应该如何预防新型冠状病毒肺炎?
日常预防一:勤洗手。无论是饭前便后,还是下班回家,一定要勤洗手,并且认真洗手。洗手时要使用肥皂或用免洗液洗手。
日常预防二:勤消毒。家里可以用乙醚、75%乙醇、含氯消毒剂、过氧乙酸和氯仿等脂溶剂做好居家消毒。家中一定要定期消毒,尤其是外出回家之后,更要注意。
日常预防三:出门一定戴好口罩,出门一定要佩戴符合国家标准的口罩如医用外科一次性口罩或N95口罩,在病毒肆虐的现实面前大家都是易感人群。
(1)佩戴口罩预防病毒相当于化学实验中的_______操作。
A 过滤 B 吸附
(2)生产N95口罩的主要原料是聚丙烯,它属于_____。
A 金属材料 B 合成材料
(3)乙醇(C2H5OH)、乙醚(C4H10O)、氯仿(CHCl3)属于______。
A 有机物 B 无机物
(4)84消毒液与含酒精的消毒剂、家中的洁厕灵等其它清洁剂混合使用,因为其有强氧化性,反应会生成有毒气体。84消毒剂具有强氧化性属于________。
A 物理性质 B 化学性质
(5)根据你的生活经验及从电视等媒体中得到的知识,写出除上述预防新型冠状病毒肺炎的方法 _____________________(写一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某碳酸钙样品中碳酸钙的质量分数,某学习小组进行了如下实验探究。取10g碳酸钙样品放入烧杯中,加入稀盐酸至不再产生气泡为止(样品中的杂质仅有 CaCl2),并绘制了加入稀盐酸的质量与放出气体质量的坐标图(如图).

(1)所用稀盐酸的溶质质量分数是多少?______
(2)该样品中碳酸钙的质量分数为多少?______
(3)当盐酸和样品恰好完全反应,所得溶液中溶质质量分数是多少?(规范写出计算过程)______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
酸奶营养丰富,富含人体生长发育所必须的多种营养物质,是人们喜爱的食品。
表 1 某品牌酸奶中主要营养成分的含量(每 100 克)
蛋白质/克 | 糖类/克 | 脂肪/克 | 钠/毫克 | 钙/毫克 |
2.7 | 9.5 | 2.7 | 75 | 90 |
但是,普通酸奶含有乳糖,经调查,我国有 88.9%的成人缺乏分解乳糖的乳糖酶,有55.1%的成年人表现有乳糖不耐受症状(主要症状为腹泻)。因此,在保证普通酸奶基本营养不损失的前提下,乳糖含量较低或无乳糖的酸奶成为乳糖不耐受消费者的需求。相关科研技术人员为满足消费者的需求,开始研发无乳糖酸奶。无乳糖酸奶的工艺流程为:原料乳 → 标准化 → 添加 6%的白砂糖 → 均质 → 巴氏杀菌 → 冷却→接种发酵剂(直投式发酵剂)→ 发酵(37℃、42℃)→ 4℃低温储存。
研究一 发酵酸奶中添加乳糖酶对乳糖水解效果的影响
在 37℃,向普通酸奶中添加不同剂量乳糖酶(剂量分别为 1000U/kg、1500U/kg、2000U/kg、2500U/kg),发酵 3 小时,测得发酵酸奶中乳糖残留量随时间的变化,如图 1 所示。
研究二 普通酸奶和无乳糖酸奶发酵过程中的酸度变化
普通酸奶和无乳糖酸奶分别在 37℃和 42℃发酵 8 小时,发酵过程中酸度(从 1 小时开始测量)变化如图 2 所示。
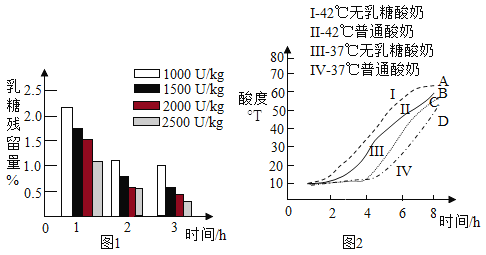
除以上研究,科技人员还在口味、活菌数、保存等方面做了无乳糖酸奶与普通酸奶的对比研究,发现无乳糖酸奶都具有一定的优势。
依据文章内容回答下列问题。
(1)由表 1 可知酸奶的主要营养成分中含量最高的是_______。
(2)由图 1 可知:3 小时内,_______(填字母序号,下同)。
A添加相同量乳糖酶,发酵酸奶中乳糖残留量随时间的延长而降低
B相同发酵时间,乳糖残留量均随乳糖酶添加量的增大而降低
C乳糖残留量与温度、时间、乳糖酶添加量有关
(3)由图 2,影响无乳糖酸奶酸度的因素是_______。
(4)由图 2 可知:42℃时无乳糖酸奶发酵过程中酸度与时间的关系是_______。
(5)下列说法正确的是_______。
A我国绝大部分成年人都有乳糖不耐受症状
B表 1 中“钠”指的是钠元素
C无乳糖酸奶的工艺中至少两步属于化学变化
D无乳糖酸奶比普通酸奶适合更多消费者食用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com