

分析 高温条件下,氧化铁和碳反应生成铁和二氧化碳,高温条件下二氧化碳和碳反应生成一氧化碳,加热条件下,一氧化碳和氧化铜反应生成铜和二氧化碳,铁和硫酸铜反应生成硫酸亚铁和铜.
解答 解:高温条件下,氧化铁和碳反应生成铁和二氧化碳,高温条件下二氧化碳和碳反应生成一氧化碳,加热条件下,一氧化碳和氧化铜反应生成铜和二氧化碳,铁和硫酸铜反应生成硫酸亚铁和铜,因此ABCDEFG分别是碳、氧化铁、二氧化碳、铁、一氧化碳、氧化铜、铜,H是可溶性铜盐;
(1)A是C,B是 Fe2O3,F是CuO.
故填:C; Fe2O3;CuO.
(2)反应①的化学方程式为:2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2.
故填:2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2.
(3)铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故填:Fe+CuSO4═FeSO4+Cu.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将植物油与水混合,得到的是溶液 | |
| B. | 物质溶解时,温度一定升高 | |
| C. | 将一杯食盐溶液倒出一多半,则倒出的溶液较稀,留在杯中的溶液较浓 | |
| D. | 食盐溶液不易结冰的原因是食盐溶液的凝固点比水低 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸不一定是化合物,碱一定是化合物 | |
| B. | 酸中一定含有氢、氧两种元素,碱中也一定含有氢、氧两种元素 | |
| C. | 酸和碱的反应一定是复分解反应,酸和碱恰好完全反应后的溶液不一定呈中性 | |
| D. | 酸不一定能与所有的金属发生反应生成盐和氢气,碱一定能与所有的盐发生反应生成新碱和新盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
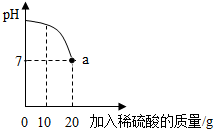 实验室有一瓶标签被腐蚀的稀硫酸溶液,小丽为了测定该稀硫酸溶液中溶质的质量分数,在烧杯中配制了16g10%的氢氧化钠溶液,然后往烧杯中滴加该稀硫酸溶液.反应过程中该溶液的pH与滴入稀硫酸溶液的质量关系如图所示.请回答下列的问题:
实验室有一瓶标签被腐蚀的稀硫酸溶液,小丽为了测定该稀硫酸溶液中溶质的质量分数,在烧杯中配制了16g10%的氢氧化钠溶液,然后往烧杯中滴加该稀硫酸溶液.反应过程中该溶液的pH与滴入稀硫酸溶液的质量关系如图所示.请回答下列的问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
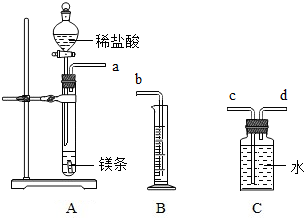 一定质量的镁与足量盐酸反应,用排水法测量产生氢气的体积,查密度表求出氢气的质量,再根据化学方程式计算出镁的相对原子质量.请利用如图给定仪器组装一套测定镁的相对原子质量的实验装置(每种仪器只用一次),并回答相关问题.
一定质量的镁与足量盐酸反应,用排水法测量产生氢气的体积,查密度表求出氢气的质量,再根据化学方程式计算出镁的相对原子质量.请利用如图给定仪器组装一套测定镁的相对原子质量的实验装置(每种仪器只用一次),并回答相关问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com