
| 98 |
| x |
| 2 |
| 0.1g |
| 4.9g |
| 20.0g |


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:初中化学 来源: 题型:
| 序号 | 样品成分 | 所选试剂 | 操作方法 |
| A | KCl(MnO2) | 水 | 溶解,过滤、洗涤、干燥 |
| B | Na2CO3(NH4HCO3) | / | 加热至质量不在减少 |
| C | NaCl(KNO3) | 水 | 溶解、降温结晶、过滤 |
| D | N2(O2) | Cu | 将气体缓缓通过足量铜网 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| 实验步骤 | 实验现象 | 实验结论及分析 |
| ①取少量滤液于试管中,滴加足量的NaOH浓溶液后加热,并将湿润的红色石蕊试纸放在试管口. | 滤液中含有NH4Cl,有关化学方程式: NaOH+NH4Cl=NaCl+NH3↑+H2O | |
| ②另取少量滤液于试管中,滴加稀盐酸. | 产生无色 无味气体. |
滤液中含有 |
| ③另取少量滤液蒸干后充分灼烧,取灼烧后的残余固体溶于水,滴加稀HNO3,再滴加AgNO3溶液. | 产生白色沉淀. | 滤液中含有 |
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀. | 反应的化学方程式: |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 纯牛奶 配料:鲜牛奶 保质朗:8个月 净含量:250mL/盒 营养成分:(每100mL) 钙≥0.11g 脂肪≥3.3g 蛋白质≥2.9g |
查看答案和解析>>
科目:初中化学 来源: 题型:
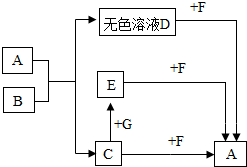 A~G均为初中常见的物质,A是一种常见的建筑材料,其中B是人体胃液中的一种酸,C是植物光合作用所需的一种原料,E是盐,F、G是碱.它们之间有如下图的相互转化关系(图中部分生成物已略去).据此推断:
A~G均为初中常见的物质,A是一种常见的建筑材料,其中B是人体胃液中的一种酸,C是植物光合作用所需的一种原料,E是盐,F、G是碱.它们之间有如下图的相互转化关系(图中部分生成物已略去).据此推断:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com