
 在宏观、微观、符号之间建立联系,是化学学科特有的思维方式.
在宏观、微观、符号之间建立联系,是化学学科特有的思维方式.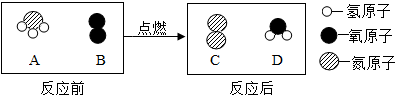
分析 (1)根据金属、大多数固态非金属单质等由原子构成,有些物质是由分子构成的,如水、氢气等,有些物质是由离子构成的,如氯化钠,进行分析解答即可.
(2)铁离子、亚铁离子是由一种原子形成的两种不同离子.
硫酸根离子、亚硫酸根离子是含有两种原子的两种不同离子;
(3)根据同种的分子化学性质相同,不同种的分子化学性质不同,进行分析解答.
物质的结构决定物质的性质,根据金刚石和石墨的物理性质不同的原因进行分析解答.
(4)根据表格提供的信息可以看出,抓住化合价数据的共性从横向上、纵向上进行分析解答本题;
(5)理解什么是等电子体,离子团所含电子数等于各离子的电子数之和;
(6)首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微粒数目关系,写出反应的方程式,然后再对题中各问加以分析解答.
解答 解:(1)C60是由C60分子构成的;金刚石属于固态非金属单质,是由碳原子直接构成的;硫酸铜是由铜离子和硫酸根离子构成的.
(2)铁离子、亚铁离子是由一种原子形成的两种不同离子,其离子符号分别是Fe2+、Fe3+.
硫酸根离子、亚硫酸根离子是含有两种原子的两种不同离子,其离子符号分别是SO32-、SO42-.
(3)一氧化碳和二氧化碳的化学性质不同,是因为它们分子的构成不同,不同种的分子化学性质不同.
金刚石和石墨的物理性质不同,是因为金刚石和石墨中碳原子的排列方式不同.
(4)根据化合物化学式的书写步骤,+6价硫元素氧化物的化学式为:SO3;
若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为=|+7|+|-1|=8;
(3)理解等电子体是具有相同原子数和电子数的分子或离子.
A、一个NO分子中有3个原子,7+8=15个电子;一个O2分子中有2个原子,8+8=16个电子,所以A中两种分子不是等电子体;
B、一个CO分子中有2个原子,6+8=14个电子;一个N2分子中有2个原子,7+7=14个电子,所以B中两种分子是等电子体;
C、一个SO2分子中有3个原子,16+8×2=32个电子;一个CO2分子中有3个原子,6+8×2=22个电子,所以C中两种分子不是等电子体;
D、H2O分子中原子数为3,而NH3分子中原子数为4,所以不是等电子体;.
故选:B;
(6)依据图示的分子结构可知该反应的化学方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
该反应中,A、C两种物质的质量变化之比为4×(14+1×3):2×14×2=17:14;
故答案为:
(1)C60;(2)①Fe2+、Fe3+; ②SO32-、SO42-.
(3)①分子的构成不同; ②碳原子排列方式不同;
(4)①SO3 ②8 (5)B
(6)①4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O; ②17:14
点评 本题难度不大,掌握常见化学用语(分子符号、离子符号等)的书写方法并能灵活运用是正确解答此类题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
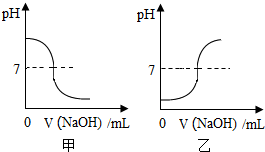 NaOH是化学实验中常用的试剂.
NaOH是化学实验中常用的试剂.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
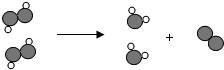 如图为某反应的部分微观示意图,其中不同的球代表不同种原子.下列说法正确的是( )
如图为某反应的部分微观示意图,其中不同的球代表不同种原子.下列说法正确的是( )| A. | 分子可分,原子不可分 | |
| B. | 反应后生成了两种新的化合物 | |
| C. | 该反应的化学方程式可表示为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | |
| D. | 反应前后原子种类发生改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验:
某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质质量 | 田 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
| A. | 该反应是化合反应 | |
| B. | 在该反应中,丙物质一定做催化剂 | |
| C. | x=9g | |
| D. | 在该反应的化学方程式中,丙、丁的化学计量数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 称 量 项 目 | 质量(g) |
| NaOH和Na2CO3的混合物 | 9.30 |
| 锥形瓶+稀盐酸质量(过量) | 141.20 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合后,第一次称量的质量 | 148.50 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合后,第二次称量的质量 | 148.30 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合后,第三次称量的质量 | 148.30 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com