把某铜锌混合物15克置于足量稀硫酸中,完全反应后生成0.4克氢气,计算该混合物里铜和锌的质量.
【答案】
分析:锌会和盐酸反应;但是铜不会和盐酸反应;写出化学方程式并代入氢气的质量计算出锌的质量,然后计算铜的质量.
解答:解:设混合物里含锌的质量为X.
Zn+H
2SO
4=ZnSO
4+H
2↑
65 2
X 0.4克
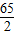
═
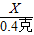
得:X=13克
∴铜的质量=15克-13克=2克.
答:该混合物里铜和锌的质量分别是2克和13克.
点评:掌握化学方程式的计算格式和规范性,注意:锌会和盐酸反应;但是铜不会和盐酸反应.
