
如图有四种微粒的结构示意图,下列有关各微粒的说法中, 不正确的是
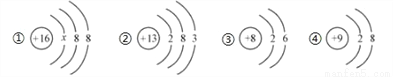
A. ①中 x=2,该粒子是一种阴离子
B. 由②的结构示意图可知,该元素在化合物中的化合价通常表现为+3 价
C. ③所示的粒子在化学反应中容易失去电子
D. ④的化学性质比较稳定
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源:广东省深圳市2019届九年级上学期期中考试化学试卷 题型:单选题
据有关资料介绍,儿童缺钙会得佝偻病,成年人缺钙会得软骨病,血液中也有少量钙,它对皮肤伤口血液的凝固起着重要作用;人体缺碘会引起甲状腺肿大。这里的“钙”、“碘”是指
A. 单质 B. 元素 C. 原子 D. 分子
查看答案和解析>>
科目:初中化学 来源:安徽省阜阳市2019届九年级第一学期第一次月考化学试卷 题型:单选题
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,从中获取的信息错误的是
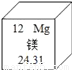
A. 该元素的原子序数为12
B. 该元素属于非金属元素
C. 该元素的原子核外有12个电子
D. 该元素的相对原子质量为24.31
查看答案和解析>>
科目:初中化学 来源:山东省济南市2019届九年级上学期12月月考化学试卷 题型:单选题
如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,下列有关说法正确的是
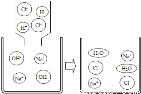
A. 反应前后,溶液的pH不变
B. 反应前后,Na+和Cl-的数目不变
C. 反应前后,H+和OH-的数目不变
D. 反应前后,H2O的数目不变
查看答案和解析>>
科目:初中化学 来源:山东省济南市2019届九年级上学期12月月考化学试卷 题型:单选题
酸溶液能使紫色石蕊试液变红色,是因为酸溶液里有
A. 氢分子 B. 氢原子 C. 氢离子 D. 水分子
查看答案和解析>>
科目:初中化学 来源:北京市2019届九年级上学期期中考试化学试卷 题型:科学探究题
过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
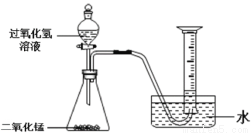
(1)如上图所示进行实验,过氧化氢分解的化学方程式为______。
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响。
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度 % | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40 min | 40 min | 40 min |
由此得出的结论是______。
Ⅱ.腐蚀性
(查阅资料)H2O2溶液有腐蚀性。
(进行实验)
同学们用铜片设计实验验证H2O2溶液的腐蚀性。(各组实验中H2O2溶液和稀硫酸所用浓度均相同)
将铜片分别浸泡在3种溶液中进行实验,如下表。
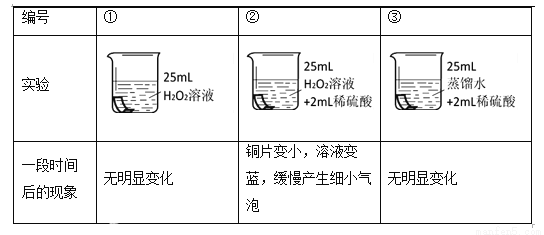
(解释与结论)
(4)实验①的作用是______。
(5)能说明铜片被腐蚀与H2O2溶液和稀硫酸均有关的实验组是______。
(6)铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu + H2O2+ H2SO4=== CuSO4 +□_______
查看答案和解析>>
科目:初中化学 来源:北京市2019届九年级上学期期中考试化学试卷 题型:填空题
变压吸附法的原理是利用分子筛吸附氮气和氧气能力的差异将二者进行分离。在吸附塔中,通过加压与减压的交替循环,可以使分子筛重复使用,部分过程的示意图如下。
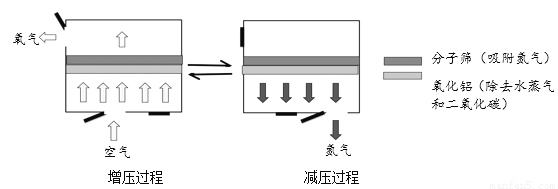
(1)分子筛中发生的变化是______(填“物理变化”或者“化学变化”)。
(2)下列说法正确的是______(填序号)。
A. 变压吸附法制取的氧气中含有稀有气体
B. 变压吸附法制取的氧气中含有二氧化碳
C. 分子筛对氮气的吸附能力与吸附塔内气体压强有关
(3)另一种分离氧气和氮气的方法是先将空气液化,再利用氮气和氧气沸点的差异进行分离。
资料:常压下,氧气的沸点是-183℃,氮气的沸点是-196℃。分离时,氮气和氧气的状态是______(填序号)。
A | B | C | D | |
氧气 | 液态 | 液态 | 气态 | 气态 |
氮气 | 液态 | 气态 | 液态 | 气态 |
查看答案和解析>>
科目:初中化学 来源:北京市2017-2018学年八年级上学期10月月考化学试卷 题型:简答题
阅读下列科普短文。
即使艳阳高照、天气晴好,有时人们也会出现眼睛刺痛、咳嗽等不良症状。专家认为,这很可能与臭氧(O3)有关。
臭氧原本是大气中自然产生的一种具有特殊臭味的微量气体,在常温常压下即可缓慢反应生成氧气,当温度达到165℃时迅速反应。绝大部分臭氧存在于离地面25公里左右处的大气平流层中,这就是人们通常所说的臭氧层。臭氧量往往随纬度、季节和天气等因素的变化而不同。研究人员发现,天空中的臭氧层能吸收99%以上的太阳紫外线,为地球上的生物提供了天然的保护屏障。为何它又成了危害健康的污染物?地表臭氧并非自然产生的,而是由石油产品(如汽油)等矿物燃料燃烧产生的氮氧化物(如二氧化氮)与空气中的氧气结合而形成的。强烈的阳光照射会加速这一化学反应。
地表空气中的臭氧对人体极为有害,一些易于过敏的人长时间暴露在臭氧含量超过每立方米180微克的环境中,会产生上述不良症状。研究表明,空气中每立方米臭氧含量增加100微克,人的呼吸功能就会减弱3%。对于运动员来说,空气中的臭氧含量可以直接影响到他们的耐力和比赛成绩。
自2013年中国执行新《环境空气质量标准》,监测6种污染物以来,臭氧便成为一些城市夏季空气质量“超标日”的首要污染物。下图为某地夏季某日昼时(7:00-18:00)臭氧、二氧化氮(NO2)浓度随时间的变化图。
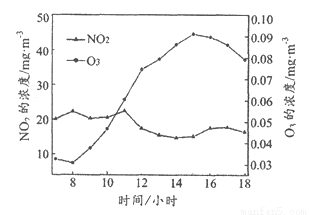
依据文章内容回答下列问题。
(1)写出臭氧的一条物理性质________。
(2)写出臭氧迅速生成氧气反应的文字表达式________。
(3)如上图,某地夏季某日昼时,臭氧污染最严重的时间段是_____(填序号)。
A.8:00~10:00 B.10:00~12:00 C.12:00~14:00 D.14:00~16:00
(4)下列说法正确的是_____(填序号)。
A.臭氧层具有吸收紫外线的作用 B.地表空气中臭氧的含量与天气阴晴无关
C.臭氧和氧气可以在不同的条件下相互转化 D.空气中臭氧浓度不同会对人体造成不同程度的影响
(5)为了减少臭氧污染,请你向市民提出一条生活中可行的倡议________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com