
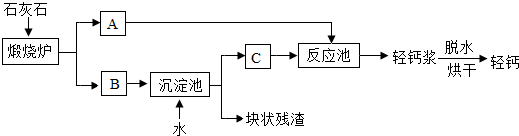
分析 (1)根据化合物中某元素的质量分数公式计算钙元素的质量分数;根据钙元素对人体的作用分析;
(2)根据碳酸钙在高温下产生氧化钙和水分析反应类型;
(3)根据碳酸钙和盐酸反应产生二氧化碳的现象分析;
(4)根据方程式的书写写出方程式.
解答 解:(1)碳酸钙中钙元素的质量分数为:$\frac{40}{100}$×100%=40%;
钙元素有助于骨骼的生长,故食盐中添加碳酸钙有助于防止人体缺钙引起的骨骼疏松症,而贫血是缺铁引起的;
(2)碳酸钙在高温下产生氧化钙和水,是一种物质生成两种物质的分解反应;
(3)碳酸钙和盐酸反应产生二氧化碳,故会观察到有气泡产生;
(4)碳酸钠和氢氧化钙反应产生碳酸钙沉淀和氢氧化钠,反应的方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
故答案为:故答案为:(1)40;贫血;
(2)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;分解反应;
(3)有气泡冒出;
(4)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
点评 本题考查了与碳酸钙有关的元素质量分数的计算、反应类型的分析、检验及化学方程式的书写,难度不大,依据相关的知识逐一分析即可.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:多选题
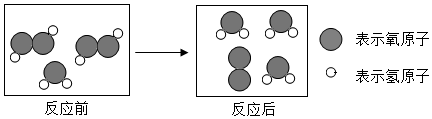
| A. | 反应前后原子种类不变 | |
| B. | 该反应是分解反应 | |
| C. | 反应后的生成物都是氧化物 | |
| D. | 该反应用化学方程式表示为2H2O2+H2O═3H2O+O2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
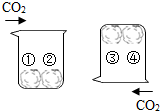 如图所示的是李梅同学探究二氧化碳性质的实验,其中①③是用紫色石蕊溶液染色的干燥的棉花团,②④是被紫色石蕊溶液浸湿的棉花团,下列说法中正确的是( )
如图所示的是李梅同学探究二氧化碳性质的实验,其中①③是用紫色石蕊溶液染色的干燥的棉花团,②④是被紫色石蕊溶液浸湿的棉花团,下列说法中正确的是( )| A. | ①③变成红色,②④不变色 | B. | ②④变成红色,①③不变色 | ||
| C. | 只有④变成红色,①②③都不变色 | D. | 只有②变成红色,①③④都不变色 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
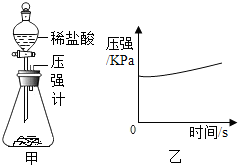 晓铭同学用如图甲所示的装置来研究铁的性质时,将一定量的铁粉置于锥形瓶底部,塞紧瓶塞,然后往锥形瓶中滴加适量的稀盐酸后,开始测量锥形瓶内部压强的变化,实验过程中锥形瓶内的压强与时间变化的关系如图乙所示:
晓铭同学用如图甲所示的装置来研究铁的性质时,将一定量的铁粉置于锥形瓶底部,塞紧瓶塞,然后往锥形瓶中滴加适量的稀盐酸后,开始测量锥形瓶内部压强的变化,实验过程中锥形瓶内的压强与时间变化的关系如图乙所示:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
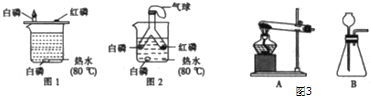
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气液化体积变小-分子体积改变 | |
| B. | 二氧化碳能灭火而一氧化碳能燃烧-原子排列方式不同 | |
| C. | 缉毒犬能根据气味发现毒品-分子在不断地运动 | |
| D. | 金刚石硬度大,石墨质软-分子构成不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲溶液中一定含有钡离子 | B. | 乙溶液中可能含有硫酸根离子 | ||
| C. | 丙溶液中一定含有氯离子 | D. | 丁溶液中一定含有钠离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com