
【题目】如图中A、B、C、D、E五种物质是初中化学常见的金属单质、非金属氧化物、酸、碱、盐中的一种,相邻物质能发生化学反应。A与B之间可发生置换反应,B的水溶液呈蓝色。请回答:
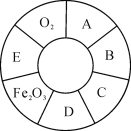
(1)A的化学式________(写一个)。
(2)B与C反应的化学方程式可能是__________。
(3)E的用途是____________。
(4)D还能与图中不相邻的一种物质反应,该反应的化学方程式可能是_________。
【答案】Fe(或Al) CuSO4+2NaOH=== Cu(OH)2↓+Na2SO4(合理即可) 冶炼金属 Fe+2HCl ===FeCl2+H2↑(或2Al+6HCl === 2AlCl3+3H2↑,与(1)中空对应,合理即可)
【解析】
A与B之间可发生置换反应,B的水溶液呈蓝色,故是铜盐溶液与活泼的金属反应生成铜,A能与氧气反应,故A可能是铁(或铝),B可能是硫酸铜,E既能与氧气反应,也能与氧化铁反应,故E可能是一氧化碳;氧化铁能与D反应,故D可能是盐酸,C既能与硫酸铜反应又能与盐酸反应,故C可能是氢氧化钠,带入框图,推断合理;
(1)A可以是铁(或铝),化学式为Fe(或Al);
(2)B是硫酸铜,C是氢氧化钠,硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,化学反应方程式:CuSO4+2NaOH=== Cu(OH)2↓+Na2SO4;
(3)E是一氧化碳,能用于冶炼金属;
(4)D是盐酸,能与不相邻的铁(或铝)反应生成氯化亚铁(或氯化铝)和氢气,化学方程式为Fe+2HCl ===FeCl2+H2↑(或2Al+6HCl === 2AlCl3+3H2↑与(1)中空对应,合理即可)。


科目:初中化学 来源: 题型:
【题目】下列反应中,属于置换反应的是
A. 2Al2O3![]() 4Al+3O2↑ B. C2H5OH+302
4Al+3O2↑ B. C2H5OH+302![]() 2CO2+3H20
2CO2+3H20
C. 2Mg+CO2![]() 2MgO+C D. AgNO3+NaCl=NaNO3+AgCl↓
2MgO+C D. AgNO3+NaCl=NaNO3+AgCl↓
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)铁是最重要的金属。
① “百炼成钢”与“铁杵磨针”蕴含的变化原理______(填“相同”或“不相同”)。
② 用图装置完成以下三个实验,每隔一段时间测量U形导管液面高度差,数据如下表。
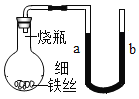
实验序号 | 瓶中盛放的物质 | 0小时 | 1小时 | 2小时 | 3小时 |
① | 干燥的铁丝 | 0cm | 0cm | 0cm | 0cm |
② | 沾食盐水的铁丝 | 0cm | 1.2cm | 5.6cm | 9.8cm |
③ | 沾了清水的铁丝 | 0cm | 0cm | 0.8cm | 3.5cm |
上述实验中,铁生锈的速率由大到小的排列顺序为(填实验序号):______。根据上述实验得出:氧气、_____、______是影响铁生锈快慢的因素。
(2)材料是时代发展的标志。
① 我国用铝合金和石墨烯混合制成的“烯合金”,有望生产出“纸一样薄的手机”。下列关于“烯合金”的说法一定错误的是______(填序号)。
A 具有可燃性 B 具有导电性 C 是一种纯净物
② 我国用铼合金制造飞机发动机叶片的技术取得重大突破,铼的原子结构示意图如图,图中X=_____。
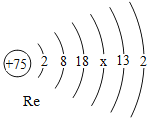
冶炼铼的化学方程式为2KReO4+7H2 ![]() 2Re+6M+2KOH,M的化学式是______。
2Re+6M+2KOH,M的化学式是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】微观示意图可以帮助我们更好地认识化学反应.下列相关认识中,错误的是
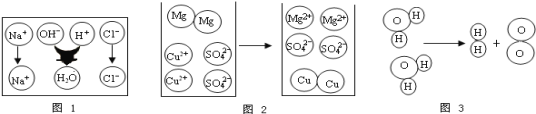
A.图1表示中和反应的实质是H+和OH-结合成水分子
B.图2表示反应的化学方程式是Mg + CuSO4 MgSO4 + Cu
C.图3表示的反应若在通电的条件下发生,说明电能可以转化为化学能
D.图3表示的反应,说明水是由氢气和氧气组成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分。它们之间的部分转化关系如下图所示(图中反应条件及部分反应物、生成物已省略)

回答下列问题:
(1)写出下列物质的化学式:A_____;B_____;C_____
(2)写出由物质C转化为物质B的化学方程式_____。
(3)写出物质C与过氧化钠(Na2O2)反应生成碳酸钠和物质A的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图回答问题。

(1)仪器①的名称:_____仪器②的名称:_____。
(2)用高锰酸钾制取氧气,可选用装置_____(选填序号)和装置D组合,反应的化学方程式为_____,若用B和D组合制取氧气,其反应的化学方程式为_____。
(3)实验室可用装置B或C制CO2,其反应的化学方程式为_____。C装置相对于B的优点有_____,用E装置收集H2,气体应从_____(选填“a”或“b”)端通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组提出可以用废锌渣(主要成分是ZnO、FeO、Fe2O3、CuO)进行适当处理可制得硫酸锌晶体(ZnSO4·x H2O)。
Ⅰ、硫酸锌晶体的制备
该兴趣小组同学设计了如下流程:

已知:①硫酸锌晶体难溶于酒精
②硫酸锌晶体受热易逐步失去结晶水
③几种物质沉淀时的pH如下表:
物质 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
开始沉淀时pH | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 3.2 | 8.0 | 6.4 |
(1)酸浸中生成硫酸锌的化学方程式为___________,属于________(填基本类型)反应。
(2)酸浸时温度和时间对锌浸出率的影响见下图。为了提高锌的浸出率,反应的最佳温度是__________℃,最佳时间是____________min;
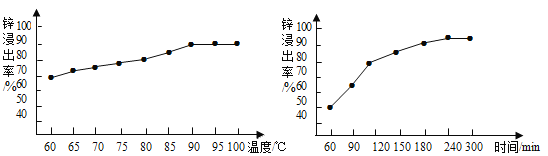
(3)加H2O2的目的是将酸浸后的Fe2+氧化成Fe3+,其反应方程式为2FeSO4 + H2O2 + _____= Fe2(SO4)3 + 2H2O,KMnO4溶液也能将Fe2+氧化成Fe3+,并生成可溶性的锰盐,选择H2O2的优点是_________;
(4)加入ZnO调节溶液的pH约为4的目的是__________;
(5)流程中,滤渣Y的成分为_________________;
(6)流程中“一系列操作”主要过程为:①_________________ 、冷却结晶、过滤,加入酒精洗涤,重复几次,最后低温烘干,得到ZnSO4·xH2O;
②用酒精洗涤的目的是洗去晶体表面的杂质、避免因水洗涤所造成的晶体损耗、_________;
③低温烘干的原因是_______________。
Ⅱ、硫酸锌晶体(ZnSO4·xH2O)组成的测定
学习小组取5.74g硫酸锌晶体(ZnSO4·xH2O)进行加热分解,获得相关数据,并绘制成剩余固体质量一温度的关系图。
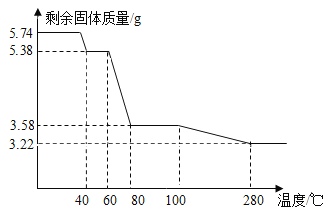
(7)280℃时,固体完全失去结晶水。根据图中数据,计算ZnSO4·xH2O中x的值为_____________;(请写出计算过程)
(8)加热过程中,硫酸锌晶体分步失去结晶水。请写出60℃到80℃时反应方程式_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石灰石是一种常见的矿物,其主要成分为碳酸钙。石灰石在工农业生产和实验室中均有重要的应用。探究小组利用石灰石开展如下实验,根据要求回答问题:
实验Ⅰ:制取二氧化碳。实验室有如下仪器装置供选择。
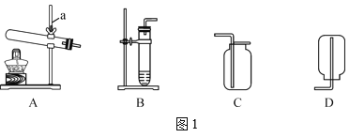
(1)仪器a的名称是______。
(2)制取和收集CO2时,应选择______和______;制取的化学方程式是______。
(3)实验过程中,为检验集气瓶中二氧化碳是否收集满,所采取的实验方法为(含操作、现象和结论)______。
实验Ⅱ:煅烧石灰石,检验分解产物。
(4)煅烧石灰石的化学方程式为______。
(5)取适量产物与足量水充分反应后静置,取上层清液通入CO2,观察到清液______,即可证明产物中含氧化钙。CO2通入清液中,所发生反应的化学方程式为______。
实验Ⅲ:研究不同温度下煅烧石灰石所得分解产物氧化钙的活性。
(6)已知:生石灰的活性受煅烧温度影响,生石灰活性越高,其化学反应能力越强。探究小组取三份等质量的石灰石样品,分别于800 ℃、900 ℃和1 000 ℃条件下煅烧15分钟,并将煅烧所得的三份固体产物分别放入盛有等质量水(足量)的三个烧杯中,测得烧杯内反应液的温度随时间的变化如图2所示。由此可推知:
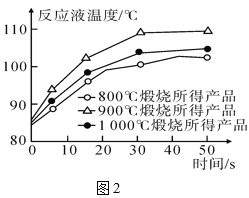
①CaO与水反应______热量(填“放出”或“吸收”);______ ℃煅烧所得CaO活性最高。
②实验时,需要控制煅烧温度、石灰石样品质量、水的用量以及______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com