
分析 根据溶液中溶质和溶剂的判断方法(即气体、固体溶于液体中,液体是溶剂,气体、固体为溶质;液体和液体相溶时,量多的为溶剂,量少的为溶质;有水时,不管量多量少,一般把水看作溶剂;没有指明溶剂时,常把水看作溶剂),稀硫酸中溶质是H2SO4 溶剂是水,锌与稀硫酸反应生成硫酸锌与氢气,欲求这种硫酸的溶质质量,需要根据参加反应的锌的质量来求,然后根据溶剂的质量=溶液的质量-溶质的质量来求溶剂的质量,据此逐一分析解答即可.
解答 解:(1)石灰水中溶质是Ca(OH)2,溶剂是水;故填:Ca(OH)2,H${\;}_{{\;}_{2}}$O;
(2)医用酒精溶液中,溶质是酒精,溶剂是水;故填:C2H5OH;H${\;}_{{\;}_{2}}$O
(3)碘酒中溶质是碘,溶剂是酒精;故填:I2;C2H5OH;
(4)硫的二硫化碳溶液里,溶质是硫,溶剂是二硫化碳;故填:S;CS2;
(5)稀硫酸中溶质是H2SO4 溶剂是水,反应后,所得溶液的质量=锌的质量+稀硫酸的质量-反应后生成的氢气的质量,
溶质的化学式为ZnSO4
设参加反应的H2SO4的质量为x;生成的ZnSO4的质量为y,反应后生成的氢气的质量为z;
Zn+H2SO4=ZnSO4+H2↑
65 98 161 2
6.5g x y z
∴$\frac{65}{6.5g}=\frac{98}{x}$,$\frac{65}{6.5g}=\frac{161}{y}=\frac{2}{z}$
解之得x=9.8g,y=16.1g z=0.2g
根据溶剂的质量=溶液的质量-溶质的质量知道,溶剂 H2O的质量=100g-9.8g=90.2g
反应后,所得溶液的质量=锌的质量+稀硫酸溶液的质量-反应后生成的氢气的质量=6.5g+100g-0.2g=106.3g
故答案为:H2SO4;9.8;H2O;90.2;106.3g; ZnSO4;16.1g.
点评 主要考查了溶液中溶质和溶剂的判断,掌握常见溶液的组成是正确解答此类题的关键所在.


科目:初中化学 来源: 题型:选择题
| A. | 大量食用高脂肪、高糖类的食物不会使人发胖 | |
| B. | 人体内的各种代谢和生理活动都离不开水,炎热的夏天更要及时补充水分 | |
| C. | 骨质疏松的中老年人饮食中应增加含铁量丰富的食物 | |
| D. | 处于生长发育期的青少年对蛋白质的需求比成年人少 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
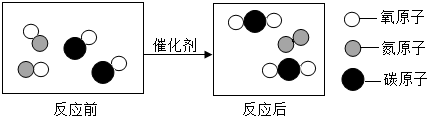 生活离不开化学,请用所学的知识解释一些问题:
生活离不开化学,请用所学的知识解释一些问题: 表示B物质的分子,B物质中碳、氧元素的质量比是3:8,6.02×1022个B分子的质量是4.4g.
表示B物质的分子,B物质中碳、氧元素的质量比是3:8,6.02×1022个B分子的质量是4.4g.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 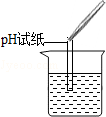 | 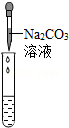 | 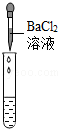 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
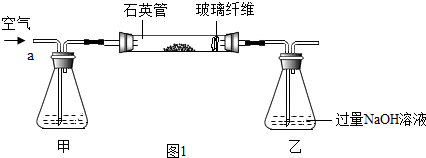
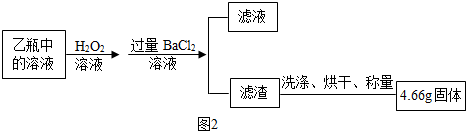
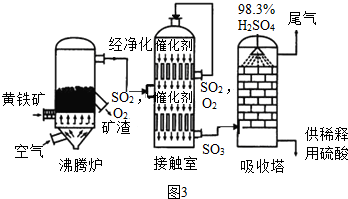
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E高温条件下可生成丙和D,D能使澄清的石灰水变浑浊.其余反应条件、部分反应物和生成物均已略去.试推断:
如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E高温条件下可生成丙和D,D能使澄清的石灰水变浑浊.其余反应条件、部分反应物和生成物均已略去.试推断:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
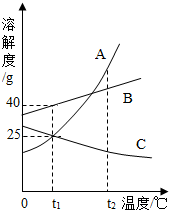 如图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
如图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )| A. | t1℃时,B物质的溶解度为40g | |
| B. | t2℃时,三种物质的溶解度由大到小的顺序为:A>B>C | |
| C. | 要使A从其浓溶液中析出,可采用冷却热饱和溶液法 | |
| D. | 要将C的不饱和溶液转化为饱和溶液可以采取降温的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com