
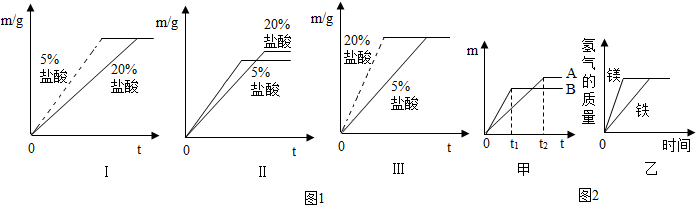
分析 (1)根据反应物种类相同时反应物浓度高反应速率快,20%的盐酸比5%的盐酸反应速率快分析;
(2)依据金属活动性顺序及同价态金属与酸反应时生成的氢气量与其相对原子质量呈反比分析判断;
(3)根据金属与酸反应的程度结合图象进行分析解答.
解答 解:(1)反应物种类相同时反应物浓度高反应速率快,20%的盐酸比5%的盐酸反应速率快,取质量相同的锌片生成的氢气质量相同,观察坐标,Ⅲ正确;故填:Ⅲ;
(2)依据金属活动性顺序表可知镁的活动性比锌强,锌的活动性比铁强,同价态三种金属与酸反应时生成的氢气量与其相对原子质量呈反比,所以取质量相等的镁片、铁片和锌片,分别放入溶质质量分数相同的足量稀盐酸中时镁产生的氢气最多,锌生成的氢气量小,因此镁反应的特点是“快而多”,坐标中没有体现出来镁的坐标;锌和铁对比,可知锌反应的特点是快而少,所以B是锌,A是铁,铁和盐酸反应产生氯化亚铁和氢气;故填:氯化亚铁;
(3)根据图示可以看出,最终生成的氢气的质量相等;
Mg+H2SO4═MgSO4+H2↑
24 98 2
Fe+2HCl═FeCl2+H2↑
56 73 2
根据反应的化学方程式以及各物质之间的质量关系可以看出,产生相同质量的氢气,消耗镁的质量小,故镁可能剩余;产生相同质量的氢气,消耗盐酸的质量小,故盐酸可能剩余;故填:①④.
点评 该题通过锌、铁、镁与盐酸之间的反应主要是考查了金属与酸的反应,只要掌握了金属与酸的反应规律以及控制变量法进行实验,便能顺利解题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验方案 | 现象与结论 |
| 观察到黑色粉末全部被磁铁吸引,说明猜想③正确. | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | 溶液变成蓝绿色 | 猜想1成立 |
| ②取少量白酒于试管中,滴入几滴紫色石蕊试液 | 石蕊试液不变色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,后用水冲洗 | |
| B. | 给试管里的药品加热时,先均匀加热,后集中加热 | |
| C. | 用滴管取细口瓶内的液体时,先将其伸入液体内,后挤压取液 | |
| D. | 向试管中装入固体粉末时,先将试管直立,后把盛药品的药匙送至试管底部 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com