
已知:Si+2NaOH+H2O=Na2SiO3+2H2↑,向100g NaOH溶液中加入足量Si,充分反应后生成0.4g H2.求:
(1)参加反应的Si的质量。
(2)该NaOH溶液中溶质的质量分数。
2.8g;8%。 【解析】根据反应的化学方程式计算解答。(1)设参加反应的Si的质量为x,该NaOH溶液中溶质的质量分数为y。 Si+2NaOH+H2O=Na2SiO3+2H2↑ 28 80 4 x 100g×y 0.4g x=2.8g y=8% 答:(1)参加反应的Si的质量为2.8g。(2)该NaOH溶液中溶质的质量分数为8%。科目:初中化学 来源:四川省广安市2018届中考化学试卷 题型:计算题
某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。

(1)图中A点表示的意义是____________________。
(2) A点消耗氢氧化钠溶液的溶质的质量为___________g。
(3)求石油产品中残余硫酸的质量___________g(写出计算过程)。
酸碱恰好中和 4 4.9g 【解析】(1)图中A点的pH=7,说明氢氧化钠和稀硫酸恰好完全反应; (2)40g氢氧化钠溶液中溶质的质量为:40g×10%=4g; (3)设石油产品中硫酸的质量为x 2 NaOH+ H2SO4= 2H2O+ Na2SO4 80 98 4g x =,解得x=4.9g查看答案和解析>>
科目:初中化学 来源:甘肃省白银、武威、定西、平凉2018年中考化学试卷 题型:填空题
生活中处处有化学。请按要求回答下列问题:
(1)自来水厂对天然水净化处理得到自来水的过程中,下列操作:①过滤;②吸附;③消毒;④蒸馏,其中没有用到的是_____。(填序号)
(2)用自来水烧水的水壶底部,容易形成水垢,水垢的成分主要是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来清除,这种调味品是_____。
(3)为了防止人体缺碘,市售食盐中添加了少量的碘酸钾(KIO3),并在使用说明中强调“不宜高温烹煮”。碘酸钾与氯酸钾性质相似,试写出碘酸钾在加热条件下分解的化学方程式_____。
④ 。 醋 。 2KIO32KI+3O2↑ 。 【解析】试题 (1)自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附、消毒等,一般用不到蒸馏。 (2)自来水烧水的水壶底部,容易形成水垢,水垢的成分主要是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来清除,这种调味品是食醋; (3)碘酸钾在加热条件下生成碘化钾和氧气,反应的化学方程式为:2KIO32KI+3O2↑。查看答案和解析>>
科目:初中化学 来源:安徽省毕业班第五次联考化学试卷 题型:实验题
根据如图实验装置回答下列问题。

(1)仪器①名称是______。写出用装置A制取氧气的化学方程式_____。该装置能否由于实验室制取二氧化碳?_______。
(2)研究显示:O2的体积分数大于36%时就可使带火星的木条复燃。因此,O2验满时采用使带火星的木条复燃的方法______(填“可靠”或“不可靠”)。为了收集一瓶较纯净的O2,最好采用的方法是______。
(3)将收集到的氧气用来做铁丝燃烧的实验,如图B,此装置存在着缺点,你的改进措施是__________。
铁架台 2KMnO4K2MnO4+MnO2+O2↑ 不能 不可靠 排水法 集气瓶底部预先放少量水或细沙 【解析】装置A是固体加热型装置,且试管略向下倾斜,试管口有棉花,所以是高锰酸钾法制取氧气,双氧水法制取氧气是固-液常温型, 实验室制取二氧化碳是固-液常温型装置,不需要酒精灯加热;(1)仪器①是铁架台。高锰酸钾法用装置A制取氧气,化学方程式为:2KMnO4K2MnO4+MnO2+O2↑。实...查看答案和解析>>
科目:初中化学 来源:安徽省毕业班第五次联考化学试卷 题型:单选题
水是生命之源泉。下列有关水的叙述正确的是
A. 用肥皂水可以将硬水转化成软水
B. 水是常见的溶剂,广泛用于工农业生产
C. 水中Ca2+、Mg2+增多会导致水中藻类植物大量生长和繁殖
D. 水是由氢原子和氧原子组成
B 【解析】 A. 用肥皂水可以将硬水和软水区分,但不能将硬水转化为软水,错误;B. 水是常见的溶剂,广泛用于工农业生产,正确;C. 植物需要的营养元素有:N、P、K,水中N、P增多会导致水中藻类植物大量生长和繁殖, 水中Ca2+、Mg2+增多会导致水的硬度增大,错误;D. 水是由氢元素和氧元素组成,水分子才是由氢原子和氧原子组成,错误。故选B。查看答案和解析>>
科目:初中化学 来源:云南省昆明市2018年中考化学试卷 题型:简答题
(1)云南很多地方都有温泉,小艳同学取某地温泉水样,冷却至室温后进行探究。
①测得温泉水样的pH=7.4,可知该温泉水样呈_____性。
②加入_____后震荡,发现泡沫较少,浮渣较多,说明该温泉水样为硬水。
③小艳同学发现长时间烧煮该温泉水的水壶中有水垢,她用厨房里的_____(填标号)轻松将水垢除去。
A.食盐水B.食醋C.料酒D.蚝油
(2)云南水资源丰富,但分布不均,节约用水,人人有责。下列不属于节水措施的是_____(填标号)。
A.使用节水龙头B.洗衣服的水用来冲厕所C.淘米的水用来浇花D.公园草坪用大水漫灌
(3)从能源能否循环再生的角度划分,煤、石油、天然气属于_____(填“可再生”或“不可再生”)能源。它们燃烧会产生SO2、CO、NO2、CO2、可吸入颗粒物等,其中没有计入空气质量日报中空气污染指数项目的是_____。随着化石燃料的日益减少,开发和利用新能源成为越来越迫切的要求。请列举出一种新能源_____。
碱 肥皂水 B ABC 不可再生 CO2 太阳能等(合理即可) 【解析】(1)①根据溶液的pH与酸碱性的关系解答;②根据生活中可用肥皂水区分软水和硬水解答;③根据水垢的主要成分是碳酸钙分析解答;(2)根据常见的节水方法分析解答;(3)根据煤、石油、天然气属于不可再生能源解答;根据计入空气质量日报中空气污染指数项目解答;根据常见新能源解答。(1)①测得温泉水样的pH=7.4,可知该温泉水样呈碱...查看答案和解析>>
科目:初中化学 来源:云南省昆明市2018年中考化学试卷 题型:单选题
在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如下表。
物质 | a | b | c | d |
反应前的质量/g | 40 | 40 | 10 | 32 |
反应后的质量/g | 12 | x | 10 | 0 |
下列说法正确的是( )
A. x等于90
B. b可能是单质
C. c一定是催化剂
D. 参加反应的a与d的质量比为7:8
D 【解析】根据质量守恒定律,在化学反应中,参加化学反应的各物质的质量总和,等于反应后生成各物质的质量总和。x=40+40+32+10-12-10=100;故a、d为反应物,b为生成物,该反应为化合反应。c的质量不变,可能为催化剂。A、x=100,错误;B、b由a、d中的元素组成,故b为化合物,错误;C、c的质量不变,可能为催化剂,错误;D、参加反应的a与d的质量比为(40-12):32=7...查看答案和解析>>
科目:初中化学 来源:宁夏2018届九年级下学期第三次模拟考试化学试卷 题型:科学探究题
小明、小芳二位同学为探究盐酸的化学性质,做了如下实验:
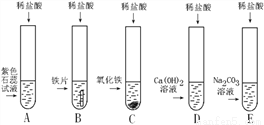
(1)试管A中的现象是____________,反应后试管B中一定有的阳离子是_________(写离子符号)。
(2)试管C中反应的化学方程式为__________________________。小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成。过滤,得到白色沉淀和无色滤液。
小芳同学欲探究无色滤液中的溶质成分:
小芳同学分析得出无色滤液中一定不含HCl,理由是________________________。
【提出问题】无色滤液的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl2;③NaCl 、CaCl2和Na2CO3;④NaCl和Na2CO3。
小明认为猜想___________一定不正确。
【进行实验】
实验步骤 | 实验现象 | 实验结论 |
①取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想_________成立 |
②取少量滤液于试管中,滴加少量______ | 有气泡产生 |
查看答案和解析>>
科目:初中化学 来源:安徽省六安市2018届九年级上学期期末考试化学试卷 题型:填空题
人类的生存与发展离不开化学.
(1)2017年5月,我国首架大型客机C919首飞,飞机材料中使用了大量的铝镁合金,铝制品具有“自我保护”能力,原因是____________________________。
(2)2017年5月,我国在南海进行了可燃冰的试开采并获得成功,天然气的主要成分为________ (填化学式),其完全燃烧的化学方程式为______________________。
(3)活性炭净化水,是利用了它的______性,生活中硬水软化的常用方法是________。
Al表面有一层致密的氧化膜 CH4 CH4 + 2O2CO2 + 2H2O 吸附性 煮沸 【解析】(1)铝制品具有“自我保护”能力,原因是铝在通常情况下能和空气中的氧气反应生成氧化铝保护膜;(2)天然气的主要成分是CH4,其完全燃烧的化学方程式为:CH4 + 2O2CO2 + 2H2O;(3)活性炭净化水,是利用了它的吸附性,生活中硬水软化的常用方法是加热煮沸,加热煮沸时,水中的钙离子、镁离...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com