
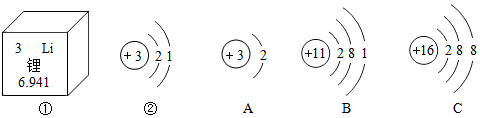
分析 (1)根据元素的分类来分析;
(2)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答;
(3)根据化合物的化学式的写法来分析;
(4)根据最外层电子数决定元素的化学性质来分析.
解答 解:(1)Li是锂元素的元素符号,锂元素属于金属元素;故填:金属;
(2)A.质子数>电子数,属于阳离子;
B.质子数=电子数,属于原子;
C.质子数<电子数,属于阴离子.
故填:C;
(3)B是钠元素,地壳中含量最高的元素是氧元素,在化合物中,钠元素显+1价,氧元素显-2价;故填:Na2O;
(4)最外层电子数决定元素的化学性质,锂原子的最外层有1个电子,与B原子的最外层电子数相同,化学性质相似,在化学反应中易失去个电子变成阳离子;故填:B.
点评 质子数决定元素的种类,最外层电子数决定元素的化学性质,依据最外层电子数可推测其得失电子的情况.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 夸克是目前发现的最小基本粒子 | B. | 质子和中子都由夸克构成 | ||
| C. | 不是所有分子中都存在夸克粒子 | D. | 夸克研究是一个科学研究的热点 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
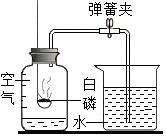
| A. | 点燃白磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞 | |
| B. | 用细铁丝代替白磷进行实验,不会影响实验结果 | |
| C. | 不打开瓶塞,聚焦太阳光引燃足量白磷,实验效果更好 | |
| D. | 若实验过程中,没有将弹簧夹夹紧,不会影响实验结果 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
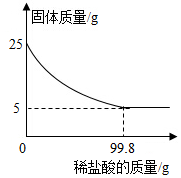 为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
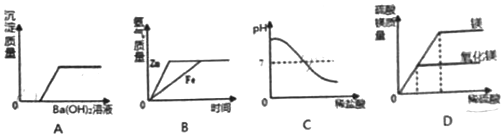
| A. | 向H2SO4和MgCl2的混合溶液中逐滴加入Ba(OH)2溶液至过量 | |
| B. | 等质量的铁和锌与足量的稀盐酸反应,产生氢气的质量与时间的关系 | |
| C. | 向一定量的氢氧化钠溶液中逐滴加入稀盐酸至恰好完全反应 | |
| D. | 等质量的镁和氧化镁固体分别与足量的稀硫酸反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com